题目内容
判断0.1 mol•L-1的NaHCO3溶液中离子浓度的大小关系。
答案:
解析:
解析:
因NaHCO3=Na++HCO
|

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
 在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )
在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )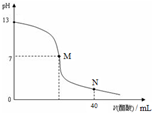 向20mL NaOH溶液中逐滴加入0.1mol/L醋酸溶液,滴定曲线如图所示.下列判断正确的是( )
向20mL NaOH溶液中逐滴加入0.1mol/L醋酸溶液,滴定曲线如图所示.下列判断正确的是( )