题目内容
下列各组物质,前者逐滴滴加到后者中直至过量,先出现白色沉淀,后来沉淀又消失的是( )
| A、H2SO4滴入NaAlO2溶液中 |
| B、Ba(OH)2溶液滴入Al2(SO4)3溶液中 |
| C、NaOH溶液滴入Al2(SO4)3溶液中 |
| D、氨水滴入Al2(SO4)3溶液中 |
考点:镁、铝的重要化合物
专题:元素及其化合物
分析:A、偏铝酸钠溶液中滴入H2SO4,先生成氢氧化铝沉淀,继续滴加氢氧化铝溶解;
B、硫酸铝溶液中滴入氢氧化钡溶液过程中一定有硫酸沉淀生成;
C、氢氧化钠溶液滴入Al2(SO4)3溶液中,开始生成氢氧化铝沉淀,继续滴加氢氧化铝溶解;
D、Al2(SO4)3溶液中滴入氨水溶液,过程中有沉淀生成,氢氧化铝不溶于过量氨水;
B、硫酸铝溶液中滴入氢氧化钡溶液过程中一定有硫酸沉淀生成;
C、氢氧化钠溶液滴入Al2(SO4)3溶液中,开始生成氢氧化铝沉淀,继续滴加氢氧化铝溶解;
D、Al2(SO4)3溶液中滴入氨水溶液,过程中有沉淀生成,氢氧化铝不溶于过量氨水;
解答:
解:A、偏铝酸钠溶液中滴入H2SO4,先生成氢氧化铝沉淀,继续滴加氢氧化铝溶解,反应的离子方程式为AlO2-+H++H2O=Al(OH)3↓;Al(OH)3+3H+=Al3++3H2O,故A符合;
B、硫酸铝溶液中滴入氢氧化钡溶液过程中一定有硫酸沉淀生成,会出现沉淀减少但不会出现沉淀全部溶解消失的现象,故B不符合;
C、氢氧化钠溶液滴入Al2(SO4)3溶液中,开始生成氢氧化铝沉淀,继续滴加氢氧化铝溶解,反应的离子方程式为,Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O,故C符合;
D、Al2(SO4)3溶液中滴入氨水溶液,过程中有沉淀生成,氢氧化铝不溶于过量氨水,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;故D不符合;
故选AC.
B、硫酸铝溶液中滴入氢氧化钡溶液过程中一定有硫酸沉淀生成,会出现沉淀减少但不会出现沉淀全部溶解消失的现象,故B不符合;
C、氢氧化钠溶液滴入Al2(SO4)3溶液中,开始生成氢氧化铝沉淀,继续滴加氢氧化铝溶解,反应的离子方程式为,Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O,故C符合;
D、Al2(SO4)3溶液中滴入氨水溶液,过程中有沉淀生成,氢氧化铝不溶于过量氨水,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;故D不符合;
故选AC.
点评:本题考查了物质性质的分析应用,物质反应滴加顺序不同产物可能不同,反应现象不同,掌握物质性质和基础是关键,题目难度中等.

练习册系列答案
相关题目
实验是化学研究的基础,下列各图所示的实验方法、装置或操作正确的是( )
A、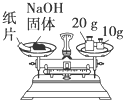 称量NaOH固体 |
B、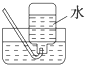 收集氯气 |
C、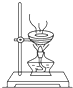 加热蒸发Nacl溶液 |
D、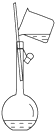 向容量瓶中转移溶液 |
在氧化还原反应5NH4NO3
2HNO3+4N2↑+9H2O中,发生氧化反应的氮原子和发生还原反应的氮原子的质量比是( )
| ||
| A、1:1 | B、5:3 |
| C、3:5 | D、1:4 |
常温下,pH=11的氨水和pH=1的盐酸等体积混合后(不考虑溶液体积微小变化),恰好完全反应,则下列说法不正确的是( )
| A、反应后所得溶液呈酸性 |
| B、混合前两溶液的物质的量浓度相等 |
| C、原氨水中约有1%的含氮粒子为NH4+ |
| D、所得溶液中NH4+、NH3?H2O与NH3三种粒子的浓度之和为0.1 mol?L-1 |
将铁片投入到下列溶液中,不放出气体并且铁片质量减轻的是( )
| A、CuCl2溶液 |
| B、HCl溶液 |
| C、NaNO3溶液 |
| D、FeCl3溶液 |
某温度下,满足下列条件的溶液肯定呈酸性的是( )
| A、加酚酞显无色的溶液 |
| B、含有H+的溶液 |
| C、pH<7的溶液 |
| D、CH3COOH和NH3?H2O混合液,当c(CH3COO-)>c(NH4+)时 |
许多氧化物在一定条件下能与Na2O2反应,反应产物很有规律,如:Na2O2+SO2=Na2SO4;Na2O2+2SO3=2Na2SO4+O2.下列化学反应方程式肯定不正确的( )
| A、2Na2O2+2Mn2O7=4NaMnO4+O2↑ |
| B、2Na2O2+2N2O3=4NaNO2+O2 |
| C、2Na2O2+2N2O5=4NaNO3+O2↑ |
| D、Na2O2+2NO2=2NaNO3+O2 |
能证明SO2具有漂白性的是( )
| A、滴入酚酞的NaOH溶液中通入SO2气体红色消失 |
| B、溴水中通入SO2气体后溶液褪色 |
| C、酸性KMnO4溶液中通入SO2气体后溶液褪色 |
| D、品红溶液中通入SO2气体红色消失 |
 将Mg条、Al条平行插入一定浓度的NaOH溶液中(如图所示连接).此电池工作时,下列叙述正确的是( )
将Mg条、Al条平行插入一定浓度的NaOH溶液中(如图所示连接).此电池工作时,下列叙述正确的是( )| A、Mg比Al活泼,失去电子被氧化成Mg2+ |
| B、Al条在反应中逐渐变细 |
| C、该电池的外电路中,电子由Mg极流出,Al极流入 |
| D、消耗24gMg,电路中将转移2mol电子 |