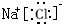题目内容
6.设NA为阿伏加德罗常数的值.下列说法不正确的是( )| A. | 由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 | |
| B. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| C. | 用石墨电极电解Cu(NO3)2溶液,当转移电子数为0.2NA时,阴极析出6.4g金属 | |
| D. | 常温下含有NA个NO2、N2O4分子的混合气体,温度降至0℃,其体积约为22.4L |
分析 A、由1mol CH3COONa和少量CH3COOH形成的中性溶液中,N(CH3COO-)+N(OH-)=N(H+)+N(Na+);
B、氮气和CO的摩尔质量均为28g/mol,且均为双原子分子;
C、当电解Cu(NO3)2溶液时,阴极上放电的是铜离子;
D、NO2气体中存在平衡:2NO2?N2O4.
解答 解:A、由1mol CH3COONa和少量CH3COOH形成的中性溶液中,N(CH3COO-)+N(OH-)=N(H+)+N(Na+),由于是中性溶液,故N(OH-)=N(H+),则N(CH3COO-)=N(Na+)=NA个,故A正确;
B、氮气和CO的摩尔质量均为28g/mol,故14g混合气体的物质的量为0.5mol,且两者均为双原子分子,故14g混合物中含NA个原子,故B正确;
C、当电解Cu(NO3)2溶液时,阴极上放电的是铜离子:Cu2++2e-=Cu,故当转移0.2NA个电子时,析出0.1mol铜即6.4g,故C正确;
D、NO2气体中存在平衡:2NO2?N2O4,反应放热,故当降温时,平衡右移,则气体的物质的量小于1mol,故体积小于22.4L,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
16.下列粒子共存的说法正确或离子方程式表达符合要求的是( )
| A. | 加入铝粉有氢气生成的溶液中可能大量存在:Ba2+、AlO2-、Cl- | |
| B. | 在含有NH3•H2O的溶液中可能大量共存的离子:Fe3+、HCO3-、NO3- | |
| C. | 亚硫酸的电离:H2SO3═HSO3-+H+ | |
| D. | 向NaHSO4溶液中加入Ba(OH)2溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
17.下列说法中,不正确的是( )
| A. | 冰融化是物理变化 | B. | 煤的干馏是化学变化 | ||
| C. | 植物通过光合作用吸收太阳能 | D. | 原子是最小的微粒,不可再分 |
14.下列关于用惰性电极电解KNO3溶液的叙述正确的是( )
| A. | 随着电解的进行,溶液的pH减小 | |
| B. | OH-向阳极移动,阳极附近溶液呈碱性 | |
| C. | 阴极上H+得电子被还原成H2 | |
| D. | NO3-向阳极移动,K+向阴极移动,分别在对应的电极上析出 |
11.为检验下列物质置于空气中是否已变质,所选试剂(括号内物质)不能达到目的是( )
| A. | FeCl2溶液(KSCN) | B. | KOH(盐酸) | ||
| C. | Na2SO3溶液(BaCl2) | D. | HCHO溶液(石蕊试液) |
18.用下列三种装置制备和收集二氧化碳气体:

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )
| A. | ①最重 | B. | ②最重 | C. | ③最重 | D. | ①②③一样重 |
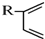 +
+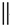 $\stackrel{△}{→}$
$\stackrel{△}{→}$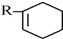
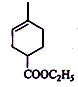 +Br2→
+Br2→ .
.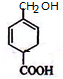 .
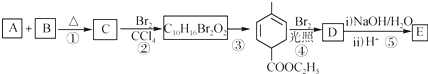
. 根据如图反应框图填空.已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.
根据如图反应框图填空.已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.