题目内容
15.对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等.下列各混合物的分离或提纯应采用什么方法?(填序号)(1)提取碘水中的碘④.
(2)除去食盐溶液中的水②.
(3)淡化海水③.
(4)除去KC1固体中含有的少量KC1O3⑤.
分析 (1)碘不易溶于水,易溶于有机溶剂;
(2)水加热时挥发;
(3)海水中水的沸点较低;
(4)不稳定,KC1O3 加热易分解.
解答 解:(1)碘不易溶于水,易溶于有机溶剂,则选择萃取法分离出碘水中的碘,故答案为:④;
(2)水加热时挥发,则选择蒸发除去食盐水中的水,故答案为:②;
(3)海水中水的沸点较低,则选择蒸馏法海水淡化,故答案为:③;
(4)不稳定,KC1O3 加热易分解,可用加热的方法除杂,故答案为:⑤.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质及常见的混合物分离提纯方法的选择为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
5.下列事故处理方法正确的是( )
| A. | 汽油失火时,立即用水灭火 | |
| B. | 实验室不小心碰翻酒精灯引起实验桌上洒落的少量酒精起火时,迅速用泡沫灭火器灭火 | |
| C. | 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 | |
| D. | 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
6.下列说法中不正确的是( )
| A. | 向沸腾的蒸馏水中逐滴加入FeCl3饱和溶液,至液体呈透明的红褐色即可制得氢氧化铁胶体 | |
| B. | 观察是一种有计划、有目的地用感官考察研究对象的方法 | |
| C. | 在豆浆中加入盐卤做豆腐利用的是胶体聚沉的原理 | |
| D. | 研究物质性质的一般程序的第一步是预测物质的性质 |
3.同温同压下,分子数相同的CO和CO2,下列说法正确的是( )
| A. | 密度之比为7:11 | B. | 体积之比为11:7 | ||
| C. | 物质的量之比为7:11 | D. | 质量之比为11:7 |
10.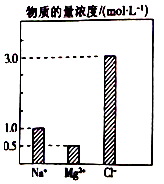 在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
 在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )| A. | NaCl的物质的量为0.2mol | |
| B. | 溶质MgCl2的质量为9 g | |
| C. | 该混合液中BaCl2的物质的量为0.1mol | |
| D. | 将该混合液加水稀释至体积为1 L,稀释后溶液中的Ba2+物质的量浓度为0.1mol/L |
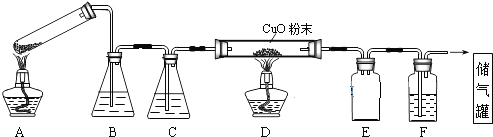
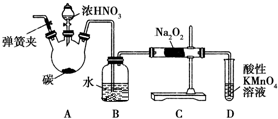 亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和铜为原料制备亚硝酸钠的装置如图所示.已知:室温下,①2NO+Na2O2═2NaNO2;②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;③酸性条件下,NO或NO2-都能与MnO4-反应生成NO3-和Mn2+.
亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和铜为原料制备亚硝酸钠的装置如图所示.已知:室温下,①2NO+Na2O2═2NaNO2;②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;③酸性条件下,NO或NO2-都能与MnO4-反应生成NO3-和Mn2+.
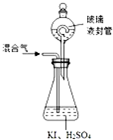 二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题: