��Ŀ����
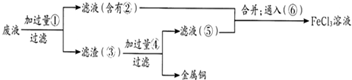
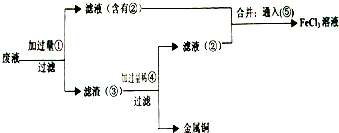
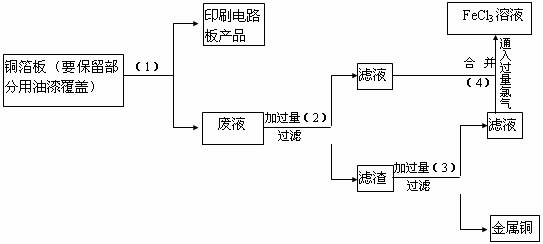
���ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�壬�ó�����ԭ�����£�FeCl3��Fe�ۡ�Cl2 ��HCl ��Ϊ��ʹFeCl3��ѭ��ʹ�ã��һ��սϹ��صĽ���ͭ��������²�������
�ش���������
��һ��������ͼ�У�1���������
�䷴Ӧ�����ӷ���ʽΪ
������������ͼ��2�����Ǽ������������ۣ�������Ӧ�����ӷ���ʽΪ
�������������ﺬ ��
�ӹ����ģ�3��������Ӧ�����ӷ���ʽΪ
����ͼ��4����Һ��������Ӧ�����ӷ���ʽΪ
���ģ�������ӡˢ��·��Ĺ�����ʵ�����ĵ�ԭ���� �� ��
��һ��30% FeCl3 ��Һ�� 2Fe3�� + Cu = Cu2�� + 2Fe2��
������Cu2�� + Fe = Cu + Fe2��
������������Fe ��Cu , Fe + 2H�� = Fe2�� + H2 ��
2Fe2�� + Cl2 = 2Fe3�� + 2Cl
���ģ�Fe Cl2 HCl

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�