题目内容
18.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失).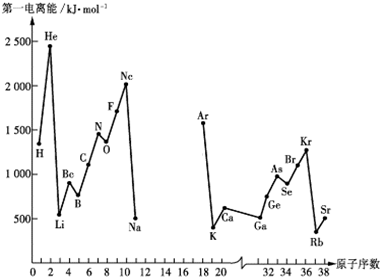
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na--Ar元素中,Al的第一电离能的大小(最小)范围为Na<Al<Mg(填元素符号).
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次减小;
(3)上图中第一电离能最小的元素在周期表中的位置是第五周期第IA族;
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有两性,其中Be(OH)2显示这种性质的离子方程式是:Be(OH)2+2H+=Be2++2H2O、Be(OH)2+2OH-=BeO2-+2H2O.
(5)单质C不可能具有的性质是D
A.具有良好的导电性
B.熔沸点很高
C.硬度较小
D.易与Br单质反应,形成的化合物分子是极性分子.
分析 (1)由图可知第ⅡA、ⅤA族元素的第一电离能有突变,因此Al的第一电离能的最小范围为Na<Al<Mg.
(2)同一主族元素原子的第一电离能I1变化规律是从上到下逐渐减小.
(3)图中第一电离能最小的元素是铷,在第五周期ⅠA族.
(4)Be(OH)2、Al(OH)3均为两性氢氧化物,二者的性质相同;
(5)C的单质有石墨和金刚石等,根据石墨和金刚石的性质分析.
解答 解:(1)由图可知第ⅡA、ⅤA族元素的第一电离能有突变,因此Al的第一电离能的最小范围为Na<Al<Mg,
故答案为:Na、Mg.
(2)同一主族元素原子的从上到下,金属性增强,容易失去电子,所以第一电离能I1变化规律是从上到下逐渐减小,
故答案为:从上到下依次减小;
(3)金属性越强,越容易失去电子,所以第一电离能越小,图中第一电离能最小的元素是铷,在第五周期第ⅠA族,
故答案为:第五周期第ⅠA族;
(4)Be(OH)2、Al(OH)3均为两性氢氧化物,都能与酸反应生成盐和水,也都能与强碱反应生成盐和水,其中Be(OH)2显示这种性质的离子方程式是Be(OH)2+2H+=Be2++2H2O;Be(OH)2+2OH-=BeO2-+2H2O;
故答案为:两性;Be(OH)2+2H+=Be2++2H2O,Be(OH)2+2OH-=BeO2-+2H2O;
(5)A.C的单质石墨是电的良导体,所以具有良好的导电性,故A正确;
B.C的单质中的金刚石属于原子晶体,金刚石的熔沸点很高,故B正确;
C.石墨的硬度较小,故C正确;
D.C的单质与溴单质不容易发生反应,形成的化合物分子CBr4是非极性分子,故D错误.
故答案为:D.
点评 本题考查了第一电离能变化的趋势,同一主族元素原子的第一电离能变化趋势为从上到下依次减小,元素周期表中常见元素的位置,同周期元素从左到右,电负性逐渐增大,题目难度不大.

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基戊烷 | ||
| C. | 3-甲基-2-乙基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
气体,这种气体是( )
| A. | H2 | B. | CO | C. | SO2 | D. | N2 |
| A. | O2-、F-、Na+、Mg2+的离子半径依次增大 | |
| B. | 硅、磷、硫、氯元素的最高正化合价依次升高 | |
| C. | HF、HCl、HBr、HI的沸点依次升高 | |
| D. | 锂、钠、钾、铷的金属性依次增强 |
| A. | 氯气可以使湿润的红色布条褪色,所以氯气具有漂白性 | |
| B. | 在配制一定浓度的溶液时未冷却溶液直接将溶液转移至容量瓶中,则浓度偏高 | |
| C. | 因为KNO3的溶解度很大,所以可以用重结晶法除去KNO3中的NaCL杂质 | |
| D. | 向饱和FeCl3溶液中逐滴滴加沸水可以制备Fe(OH)3胶体 |
| A. | 标准状况下,22.4LH2O含有的分子数为NA | |
| B. | 28gN2和N4组成的混合气体中含有的原子数为2NA | |
| C. | 1mol•L-1AlCl3溶液中含有的Cl-数为3NA | |
| D. | 将1mol CO2溶于1L水中,所得溶液中所含分子数为NA |
| A. | 次氯化钙溶液 | B. | 碳酸氢钙溶液 | C. | 石灰水 | D. | 硅酸钠溶液 |
| A. | 25.4% | B. | 50.8% | C. | 6mol/L | D. | 8.36mol/L |