题目内容
20.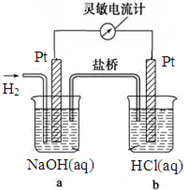 如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
分析 形成原电池反应,负极反应为H2-2e-+2OH-=2H2O,观察到b中铂电极表面有少量气泡产生,应为原电池的正极反应,电极方程式为2H++2e-=H2↑,以此解答该题.
解答 解:形成原电池反应,负极反应为H2-2e-+2OH-=2H2O,观察到b中铂电极表面有少量气泡产生,应为原电池的正极反应,电极方程式为2H++2e-=H2↑,正负极相加为OH-+H+=H2O,即总反应式为HCl+NaOH=H2O+NaCl,
故答案为:H2-2e-+2OH-=2H2O;HCl+NaOH=H2O+NaCl.
点评 本题考查了原电池的工作原理及设计原电池,为高频考点,侧重于学生的分析能力的考查,注意把握题给信息以及电极方程式的书写,难度中等.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
10.室温下,某溶液中由水电离出的c(H+)和c(OH-)的乘积是1.0×10-26,下列说法中正确的是( )
| A. | 该溶液的溶质不可能是NaHSO4 | |
| B. | 向该溶液中加入铝粉,一定能产生大量H2 | |
| C. | 下列离子在该溶液中一定能大量共存:Cl-、K+、Cu2+ | |
| D. | 向该溶液中加入NaHCO3固体,一定有化学反应发生 |
15.肉桂醛常用于牙膏、口香糖、口气清新剂等口腔护理品,其结构简式如图所示.工业上电解肉桂醇制备肉桂醛,下列说法不正确的是( )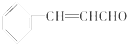
| A. | 煮沸肉桂醛与新制Cu(OH)2的混合物有砖红色沉淀生成 | |
| B. | 电解肉桂醇制得的肉桂醛在电解池的阳极生成 | |
| C. | 仅用新制银氨溶液和溴水不能鉴别肉桂醛中的碳碳双键 | |
| D. | 13.2g肉桂醛分子中含有碳碳双键数目为0.4NA |
9.实验室制取气体时,不能用排空气法收集的是( )
| A. | NO | B. | NO2 | C. | NH3 | D. | SO2 |
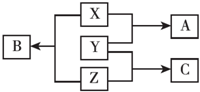 X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16,在适当条件下三种单质两两直接化合,可发生如图所示变化.已知一个B分子中含有Z元素的原子个数比C分子中的Z元素的原子个数少一个.请回答下列问题:
X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16,在适当条件下三种单质两两直接化合,可发生如图所示变化.已知一个B分子中含有Z元素的原子个数比C分子中的Z元素的原子个数少一个.请回答下列问题: ;
; 2NH3;
2NH3; 硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁.硫酸亚铁铵在 500℃时隔绝空气加热完全分解.回答下列问题:
硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁.硫酸亚铁铵在 500℃时隔绝空气加热完全分解.回答下列问题: