题目内容
2.新型净水剂高铁酸钠(Na2FeO4)可通过以下反应制备:Fe2O3+3Na2O2$\frac{\underline{\;熔融\;}}{\;}$2Na2FeO4+Na2O,下列说法正确的是( )| A. | 在Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒 | |
| B. | Na2O2既是氧化剂又是还原剂 | |
| C. | Na2FeO4既是氧化产物又是还原产物 | |
| D. | 3mol Na2O2发生反应,有12mol电子转移 |
分析 Fe2O3+3Na2O2=2Na2FeO4+Na2O中,Fe元素的化合价由+3价升高为+6价,O元素的化合价由-1价降低为-2价,以此来解答.
解答 解:A.在高铁酸钠中,铁的化合价为+6价,具有强氧化性,能杀菌消毒,故A错误;
B.Na2O2中,O元素的化合价降低,为氧化剂,故B错误;
C.Fe元素的化合价升高,O元素的化合价降低,则高铁酸钠既是氧化产物,又是还原产物,故C正确;
D.当有3molNa2O2参加反应则有3mol×2×[-1-(-2)]=6mole-发生转移,故D错误;
故选C.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念和转移电子数的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.(Ⅰ)下表是不同温度下水的离子积数据:
试回答以下问题:
(1)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=1000:1;
(2)在t2℃下,将amol•L-1CH3COOH溶液与bmol•L-1NaOH溶液等体积混合反应后,溶液恰好呈中性,则该温度下CH3COOH的电离常数Ka=$\frac{b×1{0}^{-6}}{a-b}$(用a、b表示);
(1I)已知:25℃下,下列反应;
Ag+(aq)+2NH3(aq)?Ag2(NH3)2+(aq)△H=akJ•mol-1 k=c
2Ag+(aq)+2OH-(aq)?Ag2O(s)+H2O(I)△H=blJ•mol-1 k=d
(3)写出Ag2O溶于氨水(用NH3表示)生成银氨溶液[Ag(NH3)2+]的热化学方程式:Ag2O(s)+H2O(l)+4NH3(aq)?2Ag(NH3)2+(aq)+2OH-(aq)△H=(2a-b)kJ?mol-1;计算25℃下,该反应的平衡常数(用c,d表示)k=$\frac{{c}^{2}}{d}$.
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | 1×10-13 | 1×10-12 |
(1)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=1000:1;
(2)在t2℃下,将amol•L-1CH3COOH溶液与bmol•L-1NaOH溶液等体积混合反应后,溶液恰好呈中性,则该温度下CH3COOH的电离常数Ka=$\frac{b×1{0}^{-6}}{a-b}$(用a、b表示);
(1I)已知:25℃下,下列反应;
Ag+(aq)+2NH3(aq)?Ag2(NH3)2+(aq)△H=akJ•mol-1 k=c
2Ag+(aq)+2OH-(aq)?Ag2O(s)+H2O(I)△H=blJ•mol-1 k=d
(3)写出Ag2O溶于氨水(用NH3表示)生成银氨溶液[Ag(NH3)2+]的热化学方程式:Ag2O(s)+H2O(l)+4NH3(aq)?2Ag(NH3)2+(aq)+2OH-(aq)△H=(2a-b)kJ?mol-1;计算25℃下,该反应的平衡常数(用c,d表示)k=$\frac{{c}^{2}}{d}$.
13.下列说法正确的是( )
| A. | CH3Cl和CCl4分子的空间构型均为正四面体 | |
| B. | 1,2-二氯乙烯有顺反异构体,CH3CCl=CHBr不存在顺反异构现象 | |
| C. | CH3CH=CHC≡CCF3分子中6个C原子都在同一平面上 | |
| D. | 苯的对位二元取代物只有一种说明苯分子中碳碳键不是单、双键相间交替 |
10.下列涉及有机物的说法正确的是( )
| A. | 甘油是一种油 | |
| B. | 乙烯、氯乙烯、苯乙烯都可用于合成有机高分子材料 | |
| C. | 苯能与溴发生反应,因此不能用苯萃取溴水中的溴 | |
| D. | 淀粉和纤维素水解的最终产物都是葡萄糖,因此二者互为同分异构体 |
17.下列化学用语的表述正确的是( )
| A. | Cl-的结构示意图: | B. | CCl4的电子式: | ||
| C. | 丙烯的结构简式:CH3CH2CH2 | D. | 次氯酸的结构式:H-Cl-O |
7.下列说法正确的是( )
| A. | C元素的相对分子质量是12,则1mol C的质量为12g/mol | |
| B. | 1mol Cl2的体积为22.4L | |
| C. | 1mol CO2中含有3个原子 | |
| D. | 已知NaOH溶液的物质的量浓度为0.5mol/L,则2L该溶液中含NaOH 1mol |
14.氨气在纯氧中燃烧(如图所示),生成化学性质稳定的气体X和水.下列说法正确的是( )
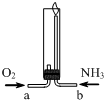

| A. | 气体X的分子式为NO | |
| B. | N2、N4为元素N的两种同素异形体 | |
| C. | 该反应条件下,氨气的还原性小于水 | |
| D. | 两种气体通入的先后顺序是NH3、O2 |
11.既可用来鉴别甲烷与乙烯,又可除去甲烷中混有乙烯的最佳方法是( )
| A. | 通入乙醇中 | B. | 通入足量溴水中 | ||
| C. | 一定条件下通入H2 | D. | 点燃 |
12.下列说法中能说明苯不是单双键交替结构的是( )
| A. | 苯的一溴代物无同分异构体 | |
| B. | 苯的间二溴代物无同分异构体 | |
| C. | 苯的对二溴代物无同分异构体 | |
| D. | 苯不能使溴水或酸性KMnO4溶液褪色 |