题目内容
14.氨气在纯氧中燃烧(如图所示),生成化学性质稳定的气体X和水.下列说法正确的是( )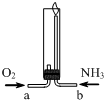
| A. | 气体X的分子式为NO | |
| B. | N2、N4为元素N的两种同素异形体 | |
| C. | 该反应条件下,氨气的还原性小于水 | |
| D. | 两种气体通入的先后顺序是NH3、O2 |
分析 氨气在纯氧中燃烧(如图所示),生成化学性质稳定的气体X和水,气体氮气,氨气与氧气反应生成氮气和水.
A.一氧化氮不稳定,容易与氧气反应;
B.同种元素组成性质不同单质,为同素异形体;
C.同一氧化还原反应中,还原剂还原性强于还原产物还原性;
D.氨气密度小于空气,氧气密度大于空气密度,要使氨气燃烧,氧气应足量;
解答 解:A.一氧化氮不稳定,与空气中氧气生成二氧化氮,与题意不符,故A错误;
B.N2、N4都是由氮元素组成,性质不同单质,二者互为同素异形体,故B正确;
C.氨气与氧气反应生成水和氮气,氨气为还原剂,水为还原产物,所以氨气的还原性大于水,故C错误;
D.氨气密度小于空气,氧气密度大于空气密度,要使氨气燃烧,氧气应足量,所以应先通入氧气,再通入氨气,故D错误;
故选:B.
点评 本题考查了元素化合物知识,明确氨气性质及同素异形体概念、氧化还原反应规律是解题关键,题目难度中等.

练习册系列答案
相关题目
4.已知A、B、C、D、E是短周期主族元素,原子序数依次增大.其中A、E的单质在常温下呈气态,B的原子最外层电子数是其电子层数的2倍,C在同周期主族元素中原子半径最大,D的周期序数与主族序数相同.下列说法正确的是( )
| A. | B位于元素周期表中第二周期第ⅥA族 | |
| B. | 工业上可以用电解CE溶液的方法同时获得C、E单质 | |
| C. | C、D的最高价氧化物对应的水化物之间能发生化学反应 | |
| D. | 化合物AE与CE具有相同类型的化学键 |
5.下列化学用语中正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 羟基的电子式: | ||
| C. | 1-丁烯的键线式: | D. | 乙醇的分子式:CH3CH2OH |
2.新型净水剂高铁酸钠(Na2FeO4)可通过以下反应制备:Fe2O3+3Na2O2$\frac{\underline{\;熔融\;}}{\;}$2Na2FeO4+Na2O,下列说法正确的是( )
| A. | 在Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒 | |
| B. | Na2O2既是氧化剂又是还原剂 | |
| C. | Na2FeO4既是氧化产物又是还原产物 | |
| D. | 3mol Na2O2发生反应,有12mol电子转移 |
9.瑞典ASES公司设计的用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,下列有关说法正确的是( )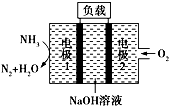

| A. | 电池工作时,电极2上发生氧化反应 | |
| B. | 电池工作一段时间后停止,溶液pH值比开始时明显增大 | |
| C. | 电极1发生的电极反应为2NH3+6OH--6e-═N2↑+6H2O | |
| D. | 用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜 |
19.下列化学变化中属于取代反应的有( )
①光照甲烷与氯气的混合气体
②由乙烯制乙醇
③乙烯使溴水褪色
④乙烯使酸性高锰酸钾褪色
⑤乙醇与乙酸的酯化反应
⑥苯与液溴在FeBr3催化下反应
⑦苯的硝化反应
⑧由乙烯制备聚乙烯.
①光照甲烷与氯气的混合气体
②由乙烯制乙醇
③乙烯使溴水褪色
④乙烯使酸性高锰酸钾褪色
⑤乙醇与乙酸的酯化反应
⑥苯与液溴在FeBr3催化下反应
⑦苯的硝化反应
⑧由乙烯制备聚乙烯.
| A. | ①⑤⑥⑦ | B. | ①③④⑦⑧ | C. | ②③④⑤⑥⑦ | D. | ①②③④⑤⑥⑦ |
6.1摩某有机物在稀硫酸作用下,水解生成2摩相同的物质.下列物质中:
①蔗糖 ②麦芽糖 ③淀粉④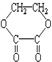 ⑤
⑤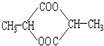 ⑥
⑥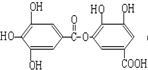 ⑦
⑦
符合题意的物质可能是( )
①蔗糖 ②麦芽糖 ③淀粉④
 ⑤
⑤ ⑥
⑥ ⑦
⑦
符合题意的物质可能是( )
| A. | ②⑤⑥⑦ | B. | ②④⑤⑦ | C. | ①②⑤⑦ | D. | ①④⑤⑥ |
3.同温下两种醋酸溶液,A溶液的物质的量浓度为c,电离度为α,B溶液的c(CH3COO-)═c,电离度为α′.下列的有关叙述中,正确的是( )
| A. | α<α′ | B. | B溶液物质的量浓度为$\frac{c}{α′}$ | ||
| C. | A溶液的pH值等于B溶液的pH值 | D. | A溶液的[H+]与B溶液的[H+]之比为1:α′ |
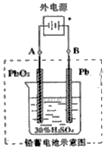 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题: