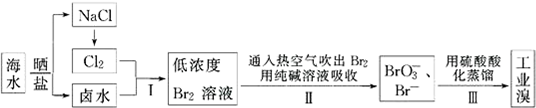
题目内容
19.下列离子与氖原子具有相同核外电子数的有( )| A. | Na+ | B. | F- | C. | Al3+ | D. | S2- |
分析 Ne原子核外电子数是10,与Ne原子具有相同的核外电子数说明该离子中核外电子数是10,阳离子核外电子数=核电荷数-所带电荷数,阴离子核外电子数=核电荷数+所带电荷数.
解答 解:Ne原子核外电子数是10,
A.钠离子核外电子数=11-1=10,故A正确;
B.氟离子核外电子数=9+1=10,故B正确;
C.铝离核外电子数=13-3=10,故C正确;
D.硫离子核外电子数=16+2=18,故D错误;
故选D.
点评 本题考查了离子核外电子数,明确阴阳离子中核外电子数的计算方法是解本题关键,题目难度不大.

练习册系列答案
相关题目
20.下列有机反应属于取代反应的是( )
| A. | nCH2═CH2-→ | B. | CH2═CH2+HCl-→CH3CH2Cl | ||
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH2CHO+2H2O | D. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$ +HBr +HBr |
10.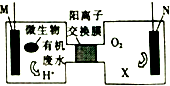 为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
 为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )
为解决淀粉厂废水中BOD严重超标的问题,有人设计了电化学降解法.如图是利用一种微生物将有机物将废水中有机物[主要成分是(C6H10O5)n]的化学能转化为电能的装置,下列说法中正确的是( )| A. | N极是负极 | |
| B. | 该装置工作时,H+从右侧经阳离子交换膜移向左侧 | |
| C. | 负极的电极反应为:(C6H10O5)n+7H2O-24ne-═6nCO2↑+24nH+ | |
| D. | 物质X是OH- |
14.将4mol A气体和2mol B气体在2L的密闭容器中混合并在一定条件下发生反应:2A(g)+B(g)?2C(g),2s时测得C的浓度为0.6mol•L-1.下列说法正确的是( )
| A. | 用物质A表示的平均反应速率为0.3mol/(L•s) | |
| B. | 用物质B表示的平均反应速率为0.6mol/(L•s) | |
| C. | 2s时物质A的转化率为70% | |
| D. | 2s时物质B的浓度为0.7mol•L-1 |
11.强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,向1L1mol•L-1的下列溶液中分别加入1L1mol•L-1的NaOH溶液:①稀醋酸;②稀硫酸;③稀盐酸,完全反应的热效应△H1、△H2、△H3的关系正确的是( )
| A. | △H1>△H2>△H3 | B. | △H1<△H3<△H2 | C. | △H1=△H3>△H2 | D. | △H2=△H3<△H1 |
8.某香料的合成原料(Y)的分子结构如图,下列有关Y的叙述正确的是( )


| A. | Y的化学式为C9H10O | |
| B. | Y可以发生加成反应和银镜反应 | |
| C. | Y分子中最多有7个碳原子处于同一平面 | |
| D. | Y的同分异构体中,属于芳香烃化合物、且苯环上仅含有一个侧链的醇类物质有5种 |
9.下列说法正确的是( )
| A. | O2和O3互为同位素 | |
| B. | X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式为H3XO4 | |
| C. | HCl的形成过程用电子式表示为 | |
| D. | 铝与稀盐酸的反应既是氧化还原反应,又是放热反应 |
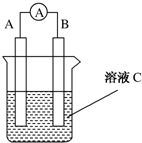 如图所示是原电池的装置图(
如图所示是原电池的装置图( 为电流表).请回答:
为电流表).请回答: