题目内容
17.下列说法正确的是( )| A. | Cl-的半径比Cl的半径小 | |
| B. | Cl2和Cl-都有毒性 | |
| C. | Cl-和Cl2都呈黄绿色 | |
| D. | Cl、HClO、Cl2及Cl-中,Cl的化学活动性最强 |
分析 A、核电荷数一样的微粒,核外电子数越多半径越大;
B、氯气有毒,但是氯离子无毒;
C、氯离子无色,氯气是黄绿色的;
D、元素的化学性质取决于原子最外层电子数,氯原子最外层7个电子,易得到电子变为氯离子.
解答 解:A、Cl-、Cl核电荷数一样的微粒,Cl-核外电子数多,半径大,故A错误;
B、氯气有毒,但是氯离子无毒,故B错误;
C、氯离子无色,氯气是黄绿色的,故C错误;
D、Cl、HClO、Cl2及Cl-中,氯原子最外层7个电子,易得到电子变为氯离子,化学活动性最强,故D正确.
故选D.
点评 本题涉及微粒之间的性质区别知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
7.为提纯下列物质(括号内物质为杂质),所选用的试剂和分离方法都正确的是( )
| 选项 | 物质 | 除杂试剂 | 分离方法或操作 |
| A | 乙醇(水) | 无水CuSO4 | 充分反应后蒸馏 |
| B | 苯(Br2) | NaOH溶液 | 振荡静置后过滤 |
| C | NaCl固体(KNO3) | 水 | 高温溶解、降温结晶 |
| D | BaCO3(BaSO4) | 饱和Na2CO3溶液 | 充分浸泡后过滤 |
| A. | A | B. | B | C. | C | D. | D |
8.下列化合物中,不含共价键的是( )
| A. | H2O | B. | NaOH | C. | MgCl2 | D. | CO2 |
5.下列叙述正确的是( )
| A. | 价电子排布为4s24p2的元素位于第四周期第ⅤA族,是P区元素 | |
| B. | 1,2-二甲苯核磁共振氢谱中有三组峰,且氢原子数之比为3:1:1 | |
| C. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 | |
| D. | 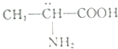 分子属于手性分子 分子属于手性分子 |
12.A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中原子半径最大的,则它们的原子序数由小到大的顺序为( )
| A. | E、B、A、D、C | B. | D、B、C、A、E | C. | E、C、D、B、A | D. | A、B、C、D、E |
14.通常用来衡量一个国家的石油化学工业发展水平的标志是( )
| A. | 石油的年产量 | B. | 硫酸的年产量 | ||
| C. | 合成纤维的年产量 | D. | 乙烯的年产量 |
15.实验室常用亚硫酸钠固体和70%的浓硫酸制备SO2气体,反应方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,请设计一套实验装置,收集一试管干燥的SO2气体.
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:
(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)
(3)某实验小组用如图乙装置测定收集到的气体中SO2的含量,反应管中装有酸性高猛酸钾溶液.
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量偏低(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积).用c、V1、V2表示SO2的体积百分含量为=$\frac{56{V}_{1}c}{56{V}_{1}c+V{\;}_{2}}$×100%.
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:

(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)
| 仪器标号 | 仪器中所加物质 | 作用 |
| A | 亚硫酸钠、浓硫酸 | 产生SO2 |
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量偏低(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积).用c、V1、V2表示SO2的体积百分含量为=$\frac{56{V}_{1}c}{56{V}_{1}c+V{\;}_{2}}$×100%.

 .
. +2C2H5OH$→_{△}^{浓硫酸}$
+2C2H5OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O. 与足量NaOH水溶液反应的化学方程式为
与足量NaOH水溶液反应的化学方程式为 .
.