题目内容
9.一定温度下,A、B能在溶液中发生反应生成C和D:A+B═C+D.a.将0.2mol•L-1A溶液和0.2mol•L-1B溶液各20mL混合;
b.将0.5mol•L-1A溶液和0.5mol•L-1B溶液各50mL混合;
c.将1mol•L-1A溶液和1mol•L-1B溶液各10mL混合,同时倒入30mL蒸馏水;
d.将20mL 1mol•L-1A溶液和60mL 1.2mol•L-1B溶液混合
反应开始时,反应速率由大到小的顺序是d>b=c>a.
分析 a.将0.2mol•L-1A溶液和0.2mol•L-1B溶液各20mL混合后A和B的浓度均为0.1mol/L;
b.将0.5mol•L-1A溶液和0.5mol•L-1B溶液各50mL混合后A和B的浓度均为0.25mol/L;
c.将1mol•L-1A溶液和1mol•L-1B溶液各10mL混合,同时倒入30mL蒸馏水,所以混合后A、B的浓度为:$\frac{1×10}{40}$=0.25mol/L;
d.将20mL 1mol•L-1A溶液和60mL 1.2mol•L-1B溶液混合后,A的浓度为$\frac{1×20}{80}$=0.25mol/L、B的浓度为:$\frac{60×1.2}{80}$=0.9mol/L,然后根据浓度越大反应速率越快,由此分析解答.
解答 解:a.将0.2mol•L-1A溶液和0.2mol•L-1B溶液各20mL混合后A和B的浓度均为0.1mol/L;
b.将0.5mol•L-1A溶液和0.5mol•L-1B溶液各50mL混合后A和B的浓度均为0.25mol/L;
c.将1mol•L-1A溶液和1mol•L-1B溶液各10mL混合,同时倒入30mL蒸馏水,所以混合后A、B的浓度为:$\frac{1×10}{40}$=0.25mol/L;
d.将20mL 1mol•L-1A溶液和60mL 1.2mol•L-1B溶液混合后,A的浓度为$\frac{1×20}{80}$=0.25mol/L、B的浓度为:$\frac{60×1.2}{80}$=0.9mol/L,然后根据浓度越大反应速率越快,所以速率由大到小的顺序为:d>b=c>a,故答案为:d>b=c>a.
点评 本题考查浓度对化学反应速率的影响,要解决其类题目首先要求溶液混合时各物质的浓度,然后根据浓度越大反应速率越快,比较容易.

| A. | 1:1000 | B. | 1:100 | C. | 1:10 | D. | 1:1 |
| A. | CH3CH2OH 和CH3OCH3 | B. | 淀粉和纤维素 | ||
| C. | 金刚石和石墨 | D. | CH3CH2CH3和CH3CH2CH2CH3 |
| A. | Cl-的半径比Cl的半径小 | |
| B. | Cl2和Cl-都有毒性 | |
| C. | Cl-和Cl2都呈黄绿色 | |
| D. | Cl、HClO、Cl2及Cl-中,Cl的化学活动性最强 |
| A. | A是固体,C是气体,正反应吸热 | B. | A是气体,C是液体,正反应放热 | ||
| C. | A是气体,C是气体,正反应放热 | D. | A是气体,C是气体,正反应吸热 |
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | a | ||||||
| 二 | b | c | d | ||||
| 三 | e | f | g | h | i | ||
| 四 | j | k | |||||
(1)写出a、e、g的元素符号:aH、eNa、gP.
(2)原子最外层电子数是最内层电子数2倍的是C,原子半径最大的是K,最高价氧化物对应水化物酸性最强的元素是Cl.
(3)剩余的元素中,离子电子层结构相同,且带电量也相同,但电性相反的两种元素是O和Mg.(以上各空均填元素符号)
(4)写出c元素单质的电子式:
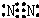 .
. | A. | S原子的结构示意图: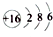 | B. | 氯化氢的电子式: | ||
| C. | 乙烯的结构式:CH2CH2 | D. | CH4分子的比例模型: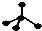 |
| A. | 化学反应能够制造出新的物质,同时也能制造出新的元素 | |
| B. | 实验室中少量金属钠、钾常保存在煤油中 | |
| C. | 葡萄酒中的花青素在碱性环境下显蓝色,故可用苏打粉检验假葡萄酒 | |
| D. | 向豆浆中加入硫酸钙会使蛋白质等聚沉制得豆腐 |
| 反应 | A | B | C | D |
| △Hl(kJ•mol-2) | 10.5 | 1.80 | -126 | -11.7 |
| △Sl(J•mol-1•K-1) | 30.0 | -113.0 | 84.0 | -105.0 |