题目内容
16.下列说法不正确的是( )| A. | 水结成冰体积膨胀,密度变小 | |
| B. | 31g白磷分子中存在的共价键数目是1.5NA(P的相对原子质量31) | |
| C. | DNA中的碱基互补配对是通过氢键来实现的 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
分析 A.水中存在氢键使分子的排列更加有序,分子间的距离增大;
B.根据白磷分子的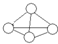 分析,每个白磷分子含有4个P原子,每个白磷分子中P-P键数目为6;
分析,每个白磷分子含有4个P原子,每个白磷分子中P-P键数目为6;
C.N元素的电负性较大,分子之间易形成氢键;
D.氢键只影响物理性质,与化学性质无关.
解答 解:A.水中存在氢键使分子的排列更加有序,分子间的距离增大,所以水结成冰体积膨胀、密度变小是氢键的作用,故A正确;
B.根据结构图 知,每个白磷分子含有4个P原子,每个白磷分子中P-P键数目为6,n(P4)=$\frac{31g}{(31×4)g/mol}$=0.25mol,31g白磷分子中存在的共价键数目=0.25mol×6×NA/mol=1.5NA,故B正确;
知,每个白磷分子含有4个P原子,每个白磷分子中P-P键数目为6,n(P4)=$\frac{31g}{(31×4)g/mol}$=0.25mol,31g白磷分子中存在的共价键数目=0.25mol×6×NA/mol=1.5NA,故B正确;
C.N元素的电负性较大,DNA中的碱基互补配对是通过氢键来实现的,故C正确;
D.H2O是一种非常稳定的化合物,与共价键有关,与氢键无关,故D错误.
故选D.
点评 本题考查了氢键的形成与性质、物质的量的计算,题目难度不大,注意氢键与分子间作用力、化学键的区别,易错点为氢键对物质性质的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列变化中,不属于化学变化的是( )
| A. | 新制氯水使有色布条褪色 | B. | 过氧化钠使某些染料褪色 | ||
| C. | 二氧化硫使品红溶液褪色 | D. | 活性炭使红墨水褪色 |
11.2,3-二甲基丁烷可生成多少种不同沸点的一溴代物( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
1.下列各组中两种微粒所含电子数不相等的是( )
| A. | H3O+和OH - | B. | CO和N2 | C. | HNO2和NO2- | D. | CO2和NO2 |
8.下列说法中正确的是( )
| A. | 元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| B. | 最外层电子数相同的元素一定属于同一族 | |
| C. | 非金属元素的最外层电子数都大于或等于4 | |
| D. | 同周期元素的电子层数相同 |
 ;比较C和D的稳定性的强弱大小H2O>NH3(用化学式表示)
;比较C和D的稳定性的强弱大小H2O>NH3(用化学式表示)