题目内容
医生通常用葡萄糖注射液维持病人血液中的血糖含量.下图是医院给病人输液时使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液的标签.
某学生欲在实验室中配制500mL该葡萄糖注射液.实验用品:葡萄糖晶体(摩尔质量为180g?mol-1)、蒸馏水、烧杯、天平、药匙、胶头滴管、量筒.
(1)实验还缺少的玻璃仪器有 .
(2)下列对容量瓶及其使用方法的描述中正确的是 .
A.使用前要检查容量瓶是否漏水
B.容量瓶用蒸馏水洗净后,再用标准葡萄糖注射液润洗
C.配制溶液时,将称好的葡萄糖晶体小心倒入容量瓶中,加蒸馏水至距刻度线1~2cm时,改用胶头滴管加蒸馏水至刻度线
D.容量瓶上标明容积、温度和浓度
(3)实验中该同学需用托盘天平称量 g葡萄糖晶体,
配制后的溶液中溶质的物质的量浓度为 .
(4)配制一定物质的量浓度的葡萄糖溶液时,下列操作使实验结果偏高的是
A.容量瓶中原有少量蒸馏水;
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中;
C.定容时观察液面俯视;
D.定容时观察液面仰视;
E.定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,所配得溶液的浓度.
| 葡萄糖注射液 |
| 规格:250mL |
| 密度:1.08g?mL-1 |
| 生产批号:10032032 |
| 有效期:至2013年3月 |
| 质量分数:5% |
(1)实验还缺少的玻璃仪器有
(2)下列对容量瓶及其使用方法的描述中正确的是
A.使用前要检查容量瓶是否漏水
B.容量瓶用蒸馏水洗净后,再用标准葡萄糖注射液润洗
C.配制溶液时,将称好的葡萄糖晶体小心倒入容量瓶中,加蒸馏水至距刻度线1~2cm时,改用胶头滴管加蒸馏水至刻度线
D.容量瓶上标明容积、温度和浓度
(3)实验中该同学需用托盘天平称量
配制后的溶液中溶质的物质的量浓度为
(4)配制一定物质的量浓度的葡萄糖溶液时,下列操作使实验结果偏高的是
A.容量瓶中原有少量蒸馏水;
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中;
C.定容时观察液面俯视;
D.定容时观察液面仰视;
E.定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,所配得溶液的浓度.
考点:配制一定物质的量浓度的溶液,计量仪器及使用方法
专题:实验题
分析:(1)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)A.使用前要检查容量瓶是否漏水;
B.容量瓶是用来配制溶液的,不需要标准葡萄糖注射液润洗;
C.根据容量瓶不能直接用来溶解固体;
D.容量瓶上标明容积、温度和规格;
(3)根据体积、密度可计算溶液的质量,再利用葡萄糖的质量分数来计算葡萄糖的质量;根据c=
来计算葡萄糖的物质的量浓度;
(4)分析操作对溶质的物质的量、溶液体积的影响,根据c=
分析操作对所配溶液浓度的影响.
(2)A.使用前要检查容量瓶是否漏水;
B.容量瓶是用来配制溶液的,不需要标准葡萄糖注射液润洗;
C.根据容量瓶不能直接用来溶解固体;
D.容量瓶上标明容积、温度和规格;
(3)根据体积、密度可计算溶液的质量,再利用葡萄糖的质量分数来计算葡萄糖的质量;根据c=
| n |
| V |
(4)分析操作对溶质的物质的量、溶液体积的影响,根据c=
| n |
| V |
解答:
解:(1)因配制一定物质的量浓度溶液步骤有:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取药品,放在小烧杯中称量,然后在烧杯中溶解(可用量筒量取水),冷却后转移到500ml容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、烧杯、药匙、玻璃棒、容量瓶、胶头滴管、500mL容量瓶,
故答案为:500mL容量瓶;
(2)A.容量瓶带有瓶塞,使用前要检查容量瓶是否漏水,故A正确;
B.用标准葡萄糖注射液润洗后,导致配制的溶液中溶质的物质的量偏大,配制的溶液浓度偏高,故B错误;
C.容量瓶为定量仪器,只能用于配制溶液,容量瓶不能用于溶解固体,故C错误;
D.容量瓶上标明容积、温度和规格,没有标注浓度,故D错误;
故选A;
(3)葡萄糖(C6H12O6)注射液的密度为1.08g?mL-1,500mL溶液,葡萄糖的质量分数5%,则含葡萄糖的质量为:500mL×1.08g/cm3×5%=27.0g,葡萄糖的物质的量为:
=0.15mol,溶质的物质的量浓度为:
=0.3mol/L,
故答案为:27.0;0.3mol/L;
(4)A.容量瓶中原有少量蒸馏水,对体积和物质的量均无影响,对所配溶液浓度无影响,故A错误;
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中,移入容量瓶内溶质的物质的量减小,所配溶液的浓度偏低,故B错误;
C.定容时观察液面俯视,导致所配溶液的体积偏小,所配溶液的浓度偏高,故C正确;
D.定容时观察液面仰视,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误;
E.定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,导致所配溶液的体积偏大,所配溶液的浓度偏小,故E错误;
故选C.
故答案为:500mL容量瓶;
(2)A.容量瓶带有瓶塞,使用前要检查容量瓶是否漏水,故A正确;
B.用标准葡萄糖注射液润洗后,导致配制的溶液中溶质的物质的量偏大,配制的溶液浓度偏高,故B错误;
C.容量瓶为定量仪器,只能用于配制溶液,容量瓶不能用于溶解固体,故C错误;
D.容量瓶上标明容积、温度和规格,没有标注浓度,故D错误;
故选A;
(3)葡萄糖(C6H12O6)注射液的密度为1.08g?mL-1,500mL溶液,葡萄糖的质量分数5%,则含葡萄糖的质量为:500mL×1.08g/cm3×5%=27.0g,葡萄糖的物质的量为:
| 27.0g |
| 180g/mol |
| 0/15mol |
| 0.5L |
故答案为:27.0;0.3mol/L;
(4)A.容量瓶中原有少量蒸馏水,对体积和物质的量均无影响,对所配溶液浓度无影响,故A错误;
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中,移入容量瓶内溶质的物质的量减小,所配溶液的浓度偏低,故B错误;
C.定容时观察液面俯视,导致所配溶液的体积偏小,所配溶液的浓度偏高,故C正确;
D.定容时观察液面仰视,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误;
E.定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,导致所配溶液的体积偏大,所配溶液的浓度偏小,故E错误;
故选C.
点评:本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,注意明确误差分析的方法

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
关于下列四个说法正确的是( )
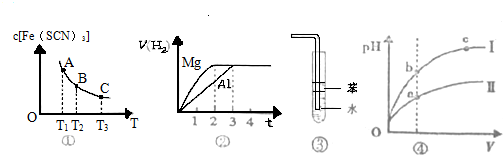

| A、已知图①是体系Fe3++3SCN-?Fe(SCB)3中c[Fe(SCN)3]与温度T的平衡图象,则A点与B点相比,A点的Fe3+浓度大 |
| B、图②表示镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积V(H2) 与时间t的关系.则反应中镁和铝的反应速率之比为2:3 |
| C、图③可用于吸收HCl气体,并防倒吸 |
| D、图④是某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的曲线,II为醋酸稀释时pH的变化曲线 |
某同学想对MnO2、CuO、Fe2O3、Cr2O3在氯酸钾分解反应中的催化作用进行如下实验:
下列叙述不正确的是( )
| 实验 编号 |
KClO3(g) | 氧化物 | 产生气体(mL) (已折算为标况) |
耗时(s) | ||
| 化学式 | 质量(g) | 实际回收 | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2(有刺激性气味) | 188.3 |
| A、催化剂的催化能力Fe2O3>MnO2>CuO |
| B、实验2、3、4中KClO3分解百分率相同 |
| C、实验1设计对本实验无意义 |
| D、Cr2O3在反应中起到还原剂作用 |
下列各物质之间的反应属于置换反应的是( )
| A、CO还原氧化铜 |
| B、钠与稀盐酸反应 |
| C、铁与稀硝酸反应 |
| D、碳与浓硫酸反应 |
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是( )
| 选项 化合物 |
A | B | C | D |
| Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
| W | MgO | Al2O3 | CO | CuCl2 |
| A、A | B、B | C、C | D、D |
如图所示与对应的叙述相符的是( )
A、 四种基本反应类型与氧化还原反应的关系 |
B、 AlCl3溶液滴加NaOH溶液生成沉淀的情况 |
C、 Ba(OH)2溶液中滴加硫酸溶液导电性的情况 |
D、 等体积等浓度稀硫酸分别与足量铁和镁反应的情况 |
 分类方法在化学学科的发展中起了非常重要的作用.图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子.对此反应的分类不正确的是( )
分类方法在化学学科的发展中起了非常重要的作用.图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子.对此反应的分类不正确的是( )| A、化合反应 | B、氧化还原反应 |
| C、可逆反应 | D、置换反应 |
 某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质.为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5g纯碱样品放人烧杯中,将烧杯放在电子称上,再把0.0g稀盐酸(足量)加入样品中.观察读数变化如下表所示:
某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质.为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5g纯碱样品放人烧杯中,将烧杯放在电子称上,再把0.0g稀盐酸(足量)加入样品中.观察读数变化如下表所示: 图中方框内区域表示所有的化学反应,大圈内区域表示氧化还原反应,大圈外区域表示非氧化还原反应,其中A~D分别表示四种基本反应类型.请分别填出:
图中方框内区域表示所有的化学反应,大圈内区域表示氧化还原反应,大圈外区域表示非氧化还原反应,其中A~D分别表示四种基本反应类型.请分别填出: