题目内容
20.等质量的钠进行下列实验,其中生成氢气最多的是( )| A. | 将钠投入到足量水中 | |
| B. | 将钠用铝箔包好并刺一些小孔,再放入足量水中 | |
| C. | 将钠放入足量稀硫酸中 | |
| D. | 将钠放入足量碳酸氢钠溶液中 |
分析 如仅是钠参加反应,无论和何种溶液反应,生成的氢气的量相等,并注意铝能与NaOH溶液反应生成氢气.
解答 解:将等质量的钠投入到水、稀硫酸、足量碳酸氢钠溶液中,放出的氢气的量相等;
将钠用铝箔包好并刺一些小孔,再放入足量的水中,首先是钠与水反应生成NaOH和氢气,铝与NaOH溶液反应生成氢气,则B项生成氢气最多,
故选B.
点评 本题考查钠的化学性质,题目难度不大,注意铝既能与酸反应又能与碱反应的性质.

练习册系列答案
相关题目
11.下列说法不正确的是( )
| A. | 互为手性异构体的分子互为镜像 | |
| B. | 利用手性催化剂合成可主要得到一种手性分子 | |
| C. | 手性异构体分子组成相同 | |
| D. | 手性异构体性质相同 |
8.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 1.0L0.1 mol/•LNa2S溶液中含有的S2-离子数为0.1NA | |
| B. | 一定条件下,4.6g的Na完全与O2反应生成7.2g产物时失去的电子数为0.2NA | |
| C. | 通过化学变化可以实现16O与18O间的相互转化 | |
| D. | 电镀铜时,若阴极得到电子数为2NA,则阳极质量减少不一定等于64g |
15.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | 二氧化碳 | 一氧化碳 | 氢氧化钠溶液和浓硫酸 | 洗气 |
| B | 硫酸钡 | 碳酸钡 | 足量的稀硫酸 | 溶解、过滤、洗涤、烘干 |
| C | 氯化钙溶液 | 消石灰 | 过量的二氧化碳 | 过滤、蒸发、结晶 |
| D | 氨气 | 水 | 火碱溶液 | 通过盛有火碱溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
12.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 1 molNa2O2溶于足量水,电子转移数为NA | |
| B. | 1L0.5mol/L C2H5OH溶液中含有的氢原子数为3NA | |
| C. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| D. | 标准状况下,2.24 LCCl4含有的共价键数为0.4NA |
9.下列表示对应化学反应的离子方程式正确的是( )
| A. | SO2通入酸性KMnO4溶液:5SO2+2H2O+2MnO4-═5SO42-+2Mn2++4H+ | |
| B. | 过量的CO2通入水玻璃中:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | NH4Al(SO4)2溶液中加入过量Ba(OH)2溶液:NH4++Al3++5OH-═NH3•H2O+AlO2-+2H2O | |
| D. | 漂白粉中加入浓盐酸:ClO-+Cl-+H2O═Cl2↑+2OH- |
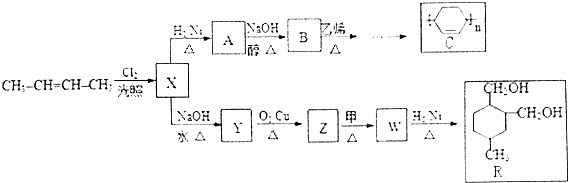
 +
+ $\stackrel{△}{→}$
$\stackrel{△}{→}$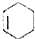
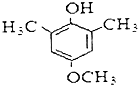 .
.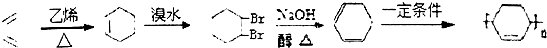 .(合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物)
.(合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B$→_{反应条件}^{反应试剂}$…目标产物)