题目内容
11.某气态烷烃和气态烯烃组成的混合气体,在相同条件下对氢气的相对密度为13;取该混合气体8.96L(标准状况)通入足量的溴水中,经充分吸收后,溴水的质量增加了5.6g,此混合气体的可能组成是( )| A. | 甲烷和丙烯 | B. | 甲烷和丁烯 | C. | 乙烷和乙烯 | D. | 丙烷和乙烯 |
分析 在同温同压下,混合气体对氢气的相对密度为13,则该混合气体的平均相对分子质量为13×2=26,据此可判断该混合气体中一定含有甲烷;
标况下8.96L混合气体的物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,则混合气体的总质量为0.4mol×26g/mol=10.4g,溴水质量增重5.6g为烯烃的质量,根据总质量可计算出甲烷的质量及物质的量,从而可知烯烃的物质的量,再根据M=$\frac{m}{n}$计算出该烯烃的摩尔质量,最后根据烯烃的通式CnH2n确定该烯烃即可.
故甲烷的质量为10.4g-5.6g=4.8g,故甲烷的物质的量为:$\frac{4.8g}{16g/mol}$=0.3mol,则烯烃的物质的量为:0.4mol-0.3mol=0.1mol,该烯烃的摩尔质量为:$\frac{5.6g}{0.1mol}$=56g/mol,设烯烃的组成为(CH2)n,则14n=56,解得:n=4,故该烯烃为丁烯.
解答 解:在同温同压下,混合气体对氢气的相对密度为13,故混合气体的平均相对分子质量为13×2=26,故一定含有甲烷;
标况下8.96L混合气体的物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,故混合气体的总质量为0.4mol×26g/mol=10.4g,溴水质量增重5.6g为烯烃的质量,故甲烷的质量为10.4g-5.6g=4.8g,故甲烷的物质的量为:$\frac{4.8g}{16g/mol}$=0.3mol,则烯烃的物质的量为:0.4mol-0.3mol=0.1mol,该烯烃的摩尔质量为:$\frac{5.6g}{0.1mol}$=56g/mol,
设烯烃的分子式为CnH2n,则14n=56,解得:n=4,故该烯烃为丁烯,
所以该混合气体为甲烷和丁烯的混合物,
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确常见有机物性质为解答关键,注意掌握相对密度与摩尔质量之间的关系,试题培养了学生的分析能力及化学计算能力.

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案| A. | 碳酸钠 | B. | 二氧化硫 | C. | 双氧水 | D. | 次氯酸钠 |
(1)测定目的:测定××牌软包装橙汁维生素C含量.
(2)测定原理:C6H8O6+I2→C6H6O6+2H++2I-.
(3)实验用品及试剂:
①仪器和用品(自选,略).
②试剂:指示剂淀粉(填名称)、浓度为7.50×10-3mol•L-1标准碘溶液、蒸馏水等.
(4)实验过程:
①洗涤仪器:检查滴定管是否漏液,润洗后装好标准碘溶液待用.
②打开橙汁包装,目测:颜色--橙黄色,澄清度--好.用酸式滴定管(或移液管)(填仪器名称)向锥形瓶中移入25.00mL待测橙汁,滴入2滴指示剂.
③用左手控制滴定管的活塞(填部位的名称),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化直到滴定终点.滴定至终点的现象是最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色.
| 滴定次数 | 待测液体积/mL | 标准碘溶液体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均值 | ||
| 1 | 25.00 | 0.00 | 14.97 | ① |
| 2 | 25.00 | 0.10 | 15.13 | |
| 3 | 25.00 | 0.22 | 14.93 | |
| A. | 两者水溶液均呈碱性,碳酸钠俗名纯碱,物质分类属于碱 | |
| B. | 两者均和稀盐酸反应产生CO2,但碳酸氢钠和盐酸反应更剧烈 | |
| C. | 用酒精灯加热时两者均可发生分解反应,但碳酸氢钠更易分解 | |
| D. | 两者均可和澄清石灰水发生反应,但碳酸氢钠反应时无沉淀 |
| A. | 常温常压下,14.2克 Na2SO4含有的Na+离子数为0.2NA | |
| B. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| C. | 通常状况下,NA个N2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为NA |
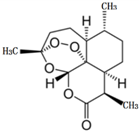 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )| A. | 青蒿素属于芳香化合物,能与H2发生加成反应 | |
| B. | 青蒿素能与氢氧化钠溶液发生反应 | |
| C. | 青蒿素的化学式为C15H22O5 | |
| D. | 青蒿素的核磁共振谱图中有12个峰 |
| A. | 蛋白质溶液 | B. | 牛奶 | C. | 盐酸 | D. | 雾 |
