题目内容
7.下列说法正确的是( )| A. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| B. | 具有相同电子层结构的四种离子A+、B2+、C-、D2-,它们的半径由大到小的顺序是D2->C->A+>B2+ | |
| C. | 分子内部一定含有共价键 | |
| D. | 族序数等于周期序数的元素一定是金属元素 |
分析 A.分子的稳定性与氢键无关;
B.A+、B2+、C-、D2-四种离子具有相同的电子层结构,核电荷数越大离子半径越小;
C.如为单原子分子,则不存在共价键;
D.H的族序数等于周期序数,但为非金属.
解答 解:A.分子的稳定性与氢键无关,决定稳定性的为共价键,而氢键属于分子间作用力,故A错误;
B.A+、B2+、C-、D2-四种离子具有相同的电子层结构,核外电子数相等,令核外电子数为x,则A、B、C、D的原子序数分别为x+1、x+2、x-1、x-2,故原子序数(核电荷数)B2+>A+>C->D2-;电子层结构相同,核电荷数越大离子半径越小,故离子半径D2->C->A+>B2+,故B正确;
C.如为单原子分子,则不存在共价键,如稀有气体,故C错误;
D.H的族序数等于周期序数,但为非金属,故D错误.
故选B.
点评 本题考查较为综合,涉及共价键,元素周期率等知识,为高频考点,侧重于学生的分析能力的考查,注意把握相关基础知识的积累.

练习册系列答案
相关题目
17.将SO2气体通入BaCl2溶液至饱和,无沉淀生成,再通入气体甲有白色沉淀生成,则气体甲可能是( )
| A. | NO | B. | NH3 | C. | CO2 | D. | HCl |
18.不粘锅的内壁有一薄层,为聚四氟乙烯.用不粘锅烹烧饭菜是不易粘锅烧焦.下列关于聚四氟乙烯的说法正确的是( )
| A. | 聚四氟乙烯分子中含有双键 | |
| B. | 聚四氟乙烯的单体是不饱和烃 | |
| C. | 聚四氟乙烯的化学性质很稳定,正常使用时不会发生化学变化 | |
| D. | 聚四氟乙烯中的氟的质量分数约为76% |
2.已知某有机物A的核磁共振氢谱如图所示,下列说法中,错误的是( )
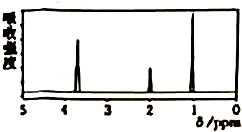

| A. | 仅由其核磁共振氢谱可知其分子中的氢原子总数由红外光谱可知,该有机物中至少含有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3 | |
| C. | 若A的化学式为C3H6O2,则其结构简式为CH3COOCH3 | |
| D. | 若A的化学式为C3H6O2,则其可能的结构有三种 |
12.下列化学用语正确的是( )
| A. | H2O2的电子式  | B. | CO2的比例模型 | ||
| C. | S2-的结构示意图 | D. | 次氯酸的结构式:H-0-Cl |
19.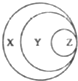 图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )
图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )
 图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )
图表归纳是学习化学的一种常用方法,某同学归纳的下表中的物质及其所属类別与图的对应关系正确的是( )| 选项 | X | Y | Z |
| A | 胶体 | 混合物 | 淀粉溶液 |
| B | 化合物 | 酸性氧化物 | 一氧化氮 |
| C | 气态氢化物 | 化合物 | 液溴 |
| D | 强电解质 | 强酸 | 硫酸 |
| A. | A | B. | B | C. | C | D. | D |
16.从海水中提取下列物质,可以不涉及化学变化的是( )
| A. | Mg | B. | Br2 | C. | NaCl | D. | K |
16.下列关于化学键的叙述正确的是( )
| A. | 离子化合物一定不含共价键 | B. | 化学键的形成与原子结构无关 | ||
| C. | 共价键只存在于共价化合物中 | D. | 离子键只存在于离子化合物中 |