题目内容
19.假设小明家的花生油不小心混入了一些水,请你利用所学知识.设计最简便的分离方法是( )| A. |  | B. |  | ||
| C. |  | D. |  |
分析 根据花生油和水是互不相溶的两种液体,分层,所以可采用分液的方法进行分离进行解答.
解答 解:花生油中不小心混入了大量的水,水与油分层,应选择分液法分离,而蒸发分离可溶性固体与液体、蒸馏分离互溶但沸点不同的液体、过滤用于分离不溶性固体和液体混合物,
故选B.
点评 本题考查物质的分离、提纯方法及选择,为高频考点,把握物质的性质及分离原理为解答的关键,注意物质性质差异及分离方法的选择,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列各项中的两个量,其比值一定为2:1的是( )
| A. | 在相同温度下,等浓度的H2SO4和CH3COOH溶液中的c(H+) | |
| B. | 相同温度下,等浓度的Ba(OH)2和NaOH溶液,前者与后者的c(OH-) | |
| C. | 相同温度下,0.2 mol•L-1醋酸溶液和0.1 mol•L-1醋酸溶液中的c(H+) | |
| D. | 液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积 |
14.下列各组物质按酸、碱、盐分类顺序排列正确的是( )
| A. | 硫酸、纯碱、食盐 | B. | 醋酸、烧碱、生石灰 | ||
| C. | 硝酸、烧碱、胆矾 | D. | 盐酸、熟石灰、氧化镁 |
4.鉴别NaCl、NaBr、NaI可以采用的试剂是( )
| A. | 碘水、淀粉溶液 | B. | 碘化钾淀粉溶液 | C. | 氯水、CCl4 | D. | 溴水、汽油 |
9.下列电离方程式正确的是( )
| A. | Ba(OH)2═Ba2++2OH- | B. | AlCl3═Al3++Cl3- | ||
| C. | H2SO4═2H++S6++4O2- | D. | Na2CO3═Na2++CO32- |
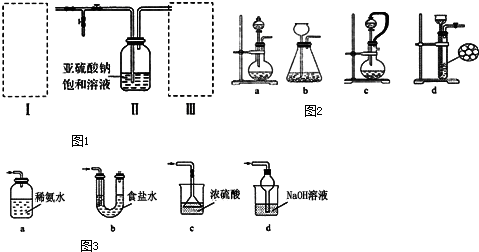
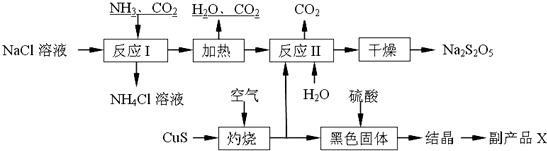
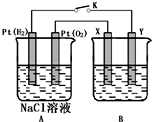 某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题: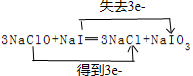 ,还原剂与氧化剂的物质的量之比是1:3.
,还原剂与氧化剂的物质的量之比是1:3.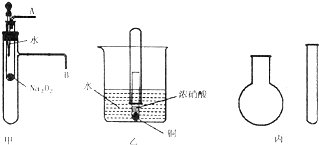 “套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验.因其具有许多优点,已被广泛应用于化学实验中.下列三个实验均为“套管实验”,请观察、分析,回答下列问题:
“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验.因其具有许多优点,已被广泛应用于化学实验中.下列三个实验均为“套管实验”,请观察、分析,回答下列问题: