题目内容
下列电子式书写正确的是( )
| A、Na:Cl | B、:N::N: |
| C、H:H | D、H:Cl |
考点:电子式
专题:化学键与晶体结构
分析:A.氯化钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
B.氮气分子中存在氮氮三键,应该存在3对共用电子对;
C.氢气分子中存在一对共用电子对;
D.氯化氢为共价化合物,分子中存在一个氢氯共用电子对,氯原子最外层一个为8个电子.
B.氮气分子中存在氮氮三键,应该存在3对共用电子对;
C.氢气分子中存在一对共用电子对;
D.氯化氢为共价化合物,分子中存在一个氢氯共用电子对,氯原子最外层一个为8个电子.
解答:
解:A.氯化钠属于离子化合物,电子式中钠离子形成离子符号形式,氯离子需要标出最外层电子,氯化钠正确的电子式为 ,故A错误;
,故A错误;
B.氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为 ,故B错误;
,故B错误;
C.氢气中存在一个H-H键,氢气的电子式为H:H,故C正确;
D.氯化氢属于共价化合物,分子中存在一个H-Cl键,氯原子最外层达到8个电子,氯化氢正确的电子式为 ,故D错误;
,故D错误;
故选C.
 ,故A错误;
,故A错误;B.氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为
 ,故B错误;
,故B错误;C.氢气中存在一个H-H键,氢气的电子式为H:H,故C正确;
D.氯化氢属于共价化合物,分子中存在一个H-Cl键,氯原子最外层达到8个电子,氯化氢正确的电子式为
 ,故D错误;
,故D错误;故选C.
点评:本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
在下列元素的原子中,次外层电子数为最外层电子数2倍的是( )
| A、核电荷数为3的元素 |
| B、核电荷数为18的元素 |
| C、核电荷数为6的元素 |
| D、核电荷数为16的元素 |
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ?mol-1 | |||
B、500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| C、氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |||
| D、氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3 |
在以下四种溶液中,各离子一定能大量共存的是( )
| A、滴加酚酞试液显红色的溶液:Fe3+、NH4+、Cl-、CO32- |
| B、含溶质为MgCl2的溶液:K+、NO3-、SO42-、Al3+ |
| C、水电离出来的c(H+)=10-13mol/L的溶液:K+、Na+、HCO3-、Br- |
| D、pH=1的溶液:Fe2+、Na+、I-、NO3- |
下列有关除杂的实验操作合理的是( )
| A、除去二氧化碳中混有的少量一氧化碳:通入适量氧气后点燃 |
| B、除去氧气中少量氮气:使气体通过炽热的铜粉 |
| C、除去石英中少量碳酸钙:用稀盐酸溶解后过滤 |
| D、除去氯化钠固体中少量的纯碱:加入足量氯化钙,过滤、蒸发、结晶 |
如图是产生和收集气体的实验装置,该装置最适合于( )
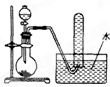

| A、用双氧水与二氧化锰反应制取O2 |
| B、用浓盐酸和MnO2反应制取Cl2 |
| C、用浓氨水和烧碱反应制取NH3 |
| D、用Na2SO3与硫酸反应制取SO2 |
它们的氯化物的化学式,最可能正确的是( )
| A、QCl2 |
| B、RCl3 |
| C、SCl2 |
| D、TCl |
 X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系.回答下列问题:
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系.回答下列问题: