题目内容
11.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.二氧化硒(Se)是一种氧剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se. 完成下列填空:(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2 2NaFeO4+2Na2O+2Na2SO4+O2↑
该反应中的氧化剂是Na2O2.简要说明K2FeO4,作为水处理剂时,在水处理过程中所起的作用高铁酸钾具有强氧化性,能杀菌消毒
消毒过程中自身被还原成铁离子,铁离子水解氢氧化铁胶体能吸附除去水中的悬浮杂质.
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO${\;}_{4}^{2-}$、C1-、H2O.每生成1molFeO${\;}_{4}^{2-}$转移3mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为0.15mo1.
(3)已知:
Se+2H2SO4(浓)2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2OSe+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是H2SO4>SeO2>SO2.
(4)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3Se+I2+KNO3+H2O ②I2+2Na2S2O3Na2S4O6+2NaI
配平方程式①,标出电子转移的方向和数目.
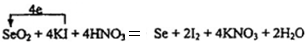 .
.
分析 (1)①2FeSO4+6Na2O2═2NaFeO4+2Na2O+2Na2SO4+O2↑中Fe元素的化合价升高,O元素的化合价既升高又降低,K2FeO4中Fe元素的化合价为+6价,具有强氧化性,且还原产物铁离子能水解;
(2)湿法制备高铁酸钾(K2FeO4),中Fe元素的化合价升高,O元素的化合价既升高又降低,根据化合价的变化来计算;
(3)自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
(4)反应①中I-失去电子生成I2,共升高2价,SeO2中+4价Se得到单质还原为单质Se,共降低4价,化合价升降最小公倍数为4,进而确定各物质的量的系数配平方程式,确定转移电子数目,标出电子转移的方向和数目.
解答 解:(1)①2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑中Fe元素的化合价升高,O元素的化合价既升高又降低,则氧化剂为Na2O2,还原剂为FeSO4,K2FeO4中Fe元素的化合价为+6价,具有强氧化性,且还原产物铁离子能水解氢氧化铁胶体,胶体具有吸附性能吸附除去水中的悬浮杂质,
故答案为:Na2O2;高铁酸钾具有强氧化性,能杀菌消毒;消毒过程中自身被还原成铁离子,铁离子水解氢氧化铁胶体能吸附除去水中的悬浮杂质;
(2)Fe元素由+3价升高到+6价,则每生成1molFeO42-转移电子为1mol×(6-3)=3mol,Cl-为还原产物,由2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O可知,若反应过程中转移了0.3mol电子,则还原产物的物质的量为0.15mol,故答案为:3;0.15;
(3)自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O中氧化剂是H2SO4、氧化产物是SeO2,所以氧化性H2SO4>SeO2,2SO2+SeO2+2H2O→Se+2SO42-+4H+中氧化剂是SeO2,还原剂是SeO2,所以氧化性SeO2>SO2,所以SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是H2SO4>SeO2>SO2,故答案为:H2SO4>SeO2>SO2;
(4)反应①中I-失去电子生成I2,共升高2价,SeO2中+4价Se得到单质还原为单质Se,共降低4价,化合价升降最小公倍数为4,故KI的系数为4,I2的系数为2,SeO2、Se的系数都是1,KNO3的系数为4,H2O的系数为2,配平并标出电子转移的方向和数目为: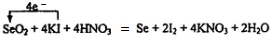 ,
,
故答案为: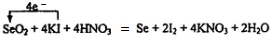 .
.
点评 本题考查氧化还原反应,明确信息及物质的性质来确定反应物与生成物是解答本题的关键,并熟悉该反应中元素的化合价来解答即可,题目难度中等.

 阅读快车系列答案
阅读快车系列答案 北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”.有一种有机物的键线式也酷似牛,如图所示,故称为牛式二烯炔醇.下列有关说法不正确的是( )
北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”.有一种有机物的键线式也酷似牛,如图所示,故称为牛式二烯炔醇.下列有关说法不正确的是( )| A. | 牛式二烯炔醇含有3种官能团 | |
| B. | 牛式二烯炔醇分子内能发生消去反应 | |
| C. | 1 mol牛式二烯炔醇最多可与6 molBr2发生加成反应 | |
| D. | 牛式二烯炔醇可发生取代反应 |
| A. | PCl3→PCl5 | B. | HNO3→NO2 | C. | S→S2- | D. | SO3→H2SO4 |
| A. | 干燥的 | B. | 以上三项均须要求的 | ||
| C. | 用欲配制的溶液润洗过的 | D. | 瓶塞不漏水的 |
| A. | ${\;}_{92}^{235}U$原子核中含有92个质子 | B. | ${\;}_{92}^{235}U$原子核外有92个电子 | ||
| C. | ${\;}_{92}^{235}U$与${\;}_{92}^{238}U$互称为核素 | D. | ${\;}_{92}^{235}U$与${\;}_{92}^{238}U$中子数不同 |
| A. | 标准状况下,22.4L水含有NA个水分子 | |
| B. | 氧气和臭氧的混合物32 g中含有NA个氧原子 | |
| C. | 7.8g Na2O2与水反应时转移0.1NA个电子 | |
| D. | 1.12L氯气中含有NA个氯原子 |
