题目内容
10.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等.按要求回答下列问题:(1)写出X的原子结构示意图
 .
.(2)列举一个事实说明W非金属性强于Z氯比硅更容易与氢气化合(或气态氢化物稳定性:HCl>SiH4或酸性:HClO4>H2SiO3或2HClO4+Na2SiO3═2NaClO4+H2SiO3↓).
(3)含Y的某种盐常用作净水剂,其净水原理是Al3++3H2O
 Al(OH)3+3H+(用离子方程式表示).
Al(OH)3+3H+(用离子方程式表示).| X | ||||
| Y | Z | W |
分析 Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知,Z为Si,X为N,W为Cl,以此来解答.
解答 解:Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知,Z为Si,X为N,W为Cl,
(1)X为N元素,核外有2个电子层,最外层电子数为5,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)比较非金属性,可根据氢化物的稳定性如HCl>SiH4,或最高价氧化物对应的酸性的强弱,如HClO4>H2SiO3或2HClO4+Na2SiO3═2NaClO4+H2SiO3↓,或与氢气反应的难易程度,
故答案为:氯比硅更容易与氢气化合(或气态氢化物稳定性:HCl>SiH4或酸性:HClO4>H2SiO3或2HClO4+Na2SiO3═2NaClO4+H2SiO3↓);
(3)Y为Al,铝离子以水解生成氢氧化铝胶体,具有吸附性,可用于净水,离子方程式为Al3++3H2O Al(OH)3+3H+,
Al(OH)3+3H+,
故答案为:Al3++3H2O Al(OH)3+3H+.
Al(OH)3+3H+.
点评 本题考查位置、结构、性质的应用,为高频考点,把握短周期元素的位置及Y的周期序数与族序数相等为解答的关键,侧重分析推断能力的考查,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
10.下列说法正确的是( )
| A. | 因为反应物浓度越大,反应速率越快,所以常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 | |
| B. | 增大反应物浓度可加快反应速度,因此用浓硫酸与铁反应能增大生成H2的速率 | |
| C. | 对化学反应速率起决定性作用的因素是参加反应的各物质的性质 | |
| D. | 化学反应速率也可以用单位时间内固体物质的消耗量或者气体物质的生成量来表示 |
18. 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )| A. | 2:3 | B. | 1:3 | C. | 3:2 | D. | 2:1 |
2. 水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸(
水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸( )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g.
常用物理常数:
请根据以上信息回答下列问题:
(1)仪器A的名称是球形冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入甲苯对合成水杨酸甲酯的作用是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率.
(3)反应结束后,分离甲醇的操作是蒸馏(或水洗分液).
(4)洗涤操作中,第一次水洗的主要目的是洗掉大部分的硫酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(5)检验产品中是否含有水杨酸的化学方法是向产品中滴加少量的紫色石蕊试液,观察是否变红.
(6)本实验的产率为59%(保留两位有效数字).
 水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸(
水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸( )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g.
常用物理常数:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是球形冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入甲苯对合成水杨酸甲酯的作用是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率.
(3)反应结束后,分离甲醇的操作是蒸馏(或水洗分液).
(4)洗涤操作中,第一次水洗的主要目的是洗掉大部分的硫酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(5)检验产品中是否含有水杨酸的化学方法是向产品中滴加少量的紫色石蕊试液,观察是否变红.
(6)本实验的产率为59%(保留两位有效数字).
19.一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g)?C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当V正(B)=2V逆(C)
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当V正(B)=2V逆(C)
| A. | ①④⑤⑥ | B. | ②③⑥ | C. | ②④⑤⑥ | D. | 只有④ |
20.对复杂的有机物结构可用“键线式”表示.如苯丙烯酸丙烯酯: 可简化为:
可简化为: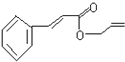 杀虫剂“阿乐丹”的结构表示为:
杀虫剂“阿乐丹”的结构表示为: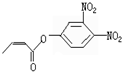 ,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
 可简化为:
可简化为: 杀虫剂“阿乐丹”的结构表示为:
杀虫剂“阿乐丹”的结构表示为: ,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )| A. | 遇FeCl3溶液均显紫色 | B. | 均能发生氧化反应 | ||
| C. | 均能与溴水发生反应 | D. | 均能与NaOH溶液发生反应 |