��Ŀ����
8����2L�ܱ������ڣ�����0.2mol NO�����0.1molO2��T��ʱ���з�Ӧ��2NO��g��+O2��g���T2NO2��g����ϵ��n��NO����ʱ��ı仯�����
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.20 | 0.10 | 0.09 | 0.08 | 0.08 | 0.08 |
��֪��K300����K350������÷�Ӧ�Ƿ��ȷ�Ӧ��
��2���ﵽƽ��ʱv��NO��Ϊ2��10-2 mol/��L•s����
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����be��
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��NO��O2��NO2��Ũ��֮��Ϊ2��1��2 d��������������ܶȱ��ֲ���
e���������������ɫ���ٱ仯
��4���ﵽƽ��ʱ�����߲���NO2��������˵����ȷ����bc��
a��ƽ�⽫�������ƶ�������Ӧ���������淴Ӧ���ʼ�С
b�����µ���ƽ��ʱ��NO��ƽ��ת���ʽ�����ƽ�ⳣ������
c�����µ���ƽ��ʱ�������ڻ��������ܶȽ�ԭ����С��ѹǿҲ��С��
���� ��1��2NO��g��+O2��g���T2NO2��g������Ӧƽ�ⳣ��K=$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$��ͼ��������֪3s�ӷ�Ӧ�ﵽƽ��״̬��������м���õ�ƽ��Ũ�ȣ�����ƽ�ⳣ���������õ���
��2����Ӧ����v��NO��=$\frac{��c}{��t}$����õ���
��3�����淴Ӧ�ﵽƽ��ʱ��v��=V�� ��ͬ�����ʱ�ʾ������������֮�ȵ��ڻ�ѧ������֮�ȣ���ͬ���ʱ�ʾ������Ӧ��������ֵ����ʵ�����Ũ�ȡ��������ٱ仯���Լ��ɴ�������һЩ��Ҳ�������仯���ɴ˽����жϣ�
��4���ﵽƽ��ʱ�����߲���NO2��ƽ��������У�
��� �⣺��1��2NO��g��+O2��g���T2NO2��g������Ӧƽ�ⳣ��K=$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$����2L�ܱ������ڣ�����0.2mol NO�����0.1molO2��T��ʱ���з�Ӧ����Ӧ�ﵽƽ��״̬�£�c��NO��=$\frac{0.08mol}{2L}$=0.04mol/L��
2NO��g��+O2��g���T2NO2��g��
��ʼ����mol/L�� 0.1 0.05 0
�仯����mol/L�� 0.06 0.03 0.06
ƽ������mol/L�� 0.04 0.02 0.06
K=$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$=$\frac{0.0{6}^{2}}{0.0{4}^{2}��0.02}$=$\frac{900}{8}$��
��֪��K300����K350�����¶�����ƽ�ⳣ����С��˵������ƽ��������У��淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ��$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��c��{O}_{2}��}$��$\frac{900}{8}$���ţ�
��2���ﵽƽ��ʱv��NO��=$\frac{0.1mol/L-0.04mol/L}{3min}$=2��10-2 mol/��L•s����
�ʴ�Ϊ��2��10-2 mol/��L•s����
��3��2NO��g��+O2��g���T2NO2��g������Ӧ�����������С�ķ��ȷ�Ӧ
a��v��NO2��=2v��O2�� ��ʾͬһ����Ӧ���ʣ�v��NO2����ʼ����Ϊv��O2����2��������˵���ﵽƽ�⣬��a����
b���淴Ӧ���У���Ӧ��������ܵ����ʵ����ڼ�С��ѹǿ֮�ȵ����������ʵ���֮�ȣ�����ѹǿ���ֲ��䣬˵����Ӧ����ƽ�⣬��b��ȷ��
c��ƽ��Ũ�Ⱥ���ʼ����ת�����йأ�NO��O2��NO2��Ũ��֮��Ϊ2��1��2������˵����Ӧ�ﵽƽ��״̬����c����
d����Ӧǰ�����������غ㣬������䣬��Ӧ�����к�ƽ��״̬�£������ܶȶ����䣬���Բ���˵����Ӧ�ﵽƽ��״̬����d����
e����Ӧ�ж������������Ǻ���ɫ���壬�������������ɫ���ٱ仯��˵��������������Ũ�Ȳ��䣬˵����Ӧ�ﵽƽ��״̬����e��ȷ��
�ʴ�Ϊ��be��
��4��a��ƽ�⽫�������ƶ�������Ӧ���ʼ�С���淴Ӧ���ʼ�С����a����
b���ﵽƽ��ʱ�����߲���NO2��ƽ��������У����µ���ƽ��ʱ��NO��ƽ��ת���ʽ�����ƽ�ⳣ�����¶ȱ仯���¶Ȳ���ƽ�ⳣ�����䣬��b��ȷ��
c���ﵽƽ��ʱ�����߲���NO2��ƽ��������У����µ���ƽ��ʱ�������ڻ������������С��������䣬�������е��ܶȽ�ԭ����С������ȫ�Զ��˼�С����������ѹǿҲ��С����c��ȷ��
�ʴ�Ϊ��b c��
���� ���⿼���˻�ѧƽ��Ӱ�����ء�ƽ���־�����жϣ�ƽ�ⳣ������Ӧ���ʵļ���Ӧ�ã����ջ������ƶ�ԭ���ǹؼ�����Ŀ�Ѷ��еȣ�

 ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�| A�� | ���Թ��еμ�Һ��ʱ����ͷ�ιܽ����Թ��ڱ� | |
| B�� | ����Fe��OH��3����ʱ��Ӧ������ˮ��FeCl3��Һ��ϼ��ȣ������Һ��ʺ��ɫ | |
| C�� | ����һ��������ͬ����ֽ����ƽ�������ϣ���Na2CO3�����������ֽ�ϳ��� | |
| D�� | ����H2SO4��Һʱ��������Ͳ�м�һ�������ˮ�����ڽ�������������Ũ���� |
| A�� | ��ʽ�ζ�����ˮϴ����δ�ñ�Һ��ϴ | |
| B�� | ��ƿ����ˮ��δ����ͼ�����������������Һ | |
| C�� | �ζ��յ�ʱ���ӵζ��ܶ��� | |
| D�� | �ζ�ʱ��Һ�ձ����ɫ������ֹͣ�ζ� |
| A�� | Ksp��AB2����Ksp��CD����������AB2���ܽ��һ��С������CD���ܽ�� | |
| B�� | ���Ȼ����ij����ܽ�ƽ����ϵ�У���������ˮ���Ȼ�����Ksp���� | |
| C�� | ���Ȼ����ij����ܽ�ƽ����ϵ�У�����⻯�ع��壬�Ȼ���������ת��Ϊ�⻯�� | |
| D�� | ��̼��Ƶij����ܽ�ƽ����ϵ�У�����ϡ���ᣬ�ܽ�ƽ�ⲻ�ƶ� |
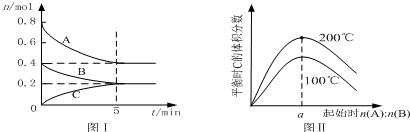
| A�� | 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v��B��=0.04 mol•L-1•min-1 | |
| B�� | ͼ����֪��ӦxA��g��+yB��g��?zC��g���ġ�H��0����a=2 | |
| C�� | ����ͼ����ʾ��ƽ��״̬�£�������ϵ�г���He�����´ﵽƽ��ǰv��������v���棩 | |
| D�� | 200��ʱ���������г���2 mol A ��1 mol B���ﵽƽ��ʱ��A ���������С��0.5 |
��1��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������400mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ����
| ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
| ���������mL������״���� | 100 | 240 | 464 | 576 | 620 |
����3��4����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����0.025mol/��L•min����
������Һ������䣩
��2����һѧ��Ҳ��ͬ����ʵ�飬���ڷ�Ӧ̫�죬���ÿ��Ʋ�������������������������м���������������Һ�Լ�����Ӧ���ʣ�����Ϊ�����е���CD��
A������ˮ B��KCl��Һ C��KNO3��Һ D��CuSO4��Һ
��3��ij�¶�����4L�ܱ������У�3����̬���� X��Y��Z�����ʵ�����ʱ��仯��������ͼ��

�ٸ÷�Ӧ�Ļ�ѧ����ʽ��3X+Y?2Z��
����5minʱ���÷�Ӧ�ﵽ��ƽ��״̬�����п���Ϊ�жϷ�Ӧ�Ѵﵽ��״̬����CD��
A��X��Y��Z�ķ�Ӧ�������
B��X��Y�ķ�Ӧ���ʱ�Ϊ3��1
C������������ѹǿ���ֲ���
D������1mol Y��ͬʱ����2mol Z
��2min��X��ת����Ϊ30%��
����������Ӧ��X��Y��Z�ֱ�ΪH2��N2��NH3������֪17g�����ֽ�ɵ���������Ҫ����46kJ��������÷�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-92kJ/mol��
��1��ʵ���ã�5g�״���CH3OH��Һ���������г��ȼ�����ɶ�����̼�����Һ̬ˮʱ�ͷų�113.5kJ�����������ʾ�״���ȼ���ȵ��Ȼ�ѧ����Ϊ��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l����H=-1452.8kJ/mol��
��2���������������Ȼ�ѧ����ʽ��?��a��b�����������=��������
2H2��g��+O2��g���T2H2O��g����H1=a kJ•mol-1?
2H2��g��+O2��g���T2H2O��l����H2=b kJ•mol-1?
��3��
| ��ѧ�� | H-H | N-H | N��N |
| ����/kJ•mol-1 | 436 | 391 | 945 |
��4�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�Ƚ������㣮����ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g���TCH3OH��g����H=-90.8kJ•mol-1[
��2CH3OH��g���TCH3OCH3��g��+H2O��g����H=-23.5kJ•mol-1
��CO��g��+H2O��g���TCO2��g��+H2��g����H=-41.3kJ•mol-1
�ܷ�Ӧ��3H2��g��+3CO��g���TCH3OCH3��g��+CO2��g���ġ�H=-246.4 kJ•mol-1��
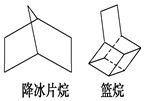 ��ͼ���Ǽ�̼�ܽṹ��
��ͼ���Ǽ�̼�ܽṹ��