��Ŀ����
��12����ͼ�е�ÿһ�����ڱ�ʾһ�ַ�Ӧ���������,����A��C��D��E��F��ͨ������¾�Ϊ���壬��A��C���ʵ���֮��Ϊ1:1��BΪ����Һ�塣

�Իش���������:
��1��X�� ��F�� (���ѧʽ)��
��2��A D��Ӧ�Ļ�ѧ����ʽ ��
D��Ӧ�Ļ�ѧ����ʽ ��
��3��G��Cu�ķ�Ӧ�У�G���ֵ������� ��
��4��X�����NaOH��Һ��Ӧ�����ȣ������ӷ���ʽ ��
��5����C��B��DΪԭ�Ͽ�����G����ʹa mol C ��ȫת��ΪG��������������ҪD mol��
(1) NH4HCO3 ; NH3 (2) 2Na2O2 +2CO2 =2Na2CO3 +O2��3�������Ժ����� ��4��NH4+ + HCO3- +2OH- 2H2O+ CO32- +NH3�� ��5��2a
2H2O+ CO32- +NH3�� ��5��2a
��������
���������A��C��D��E��F��ͨ������¾�Ϊ���壬A�ǿ��Ժ�Na2O2��Ӧ�����壬��������CO2�����ɵ�DΪO2��X���Ժ����ᷴӦ����CO2��X��̼���λ�̼�����Σ�X���Ժ�NaOH��Ӧ�������壬��X����������Σ�X����A��C���ʵ���֮��Ϊ1:1����X��NH4HCO3 ����ôB��H2O��C��NH3 ��E��NO��O2��NO��Ӧ����F��NO2��B��H2O����ôG��HNO3�����������ƶϣ���1��X��NH4HCO3�� F��NH3��2��A����D�Ļ�ѧ����ʽΪ��2Na2O2 +2CO2 =2Na2CO3 +O2��3��G��HNO3����ͭ��Ӧ������ǿ�����Ժ����ԡ���4��NH4HCO3 �����NaOH��Һ��Ӧ�����ȣ������ӷ���ʽΪ��NH4+ + HCO3- +2OH- 2H2O+ CO32- +NH3����5�����ݵ����غ��У�a molNH3��ΪHNO3ת�Ƶĵ���Ϊ8amol��ת��8amol���ӵĻ���Ҫ��ӦO2����Ϊ2a mol.
2H2O+ CO32- +NH3����5�����ݵ����غ��У�a molNH3��ΪHNO3ת�Ƶĵ���Ϊ8amol��ת��8amol���ӵĻ���Ҫ��ӦO2����Ϊ2a mol.
���㣺���ʵ��ƶϡ����ӷ���ʽ����д��������ԭ��Ӧ�еĵ����غ�����á�

���ݱ�����Ϣ���ж�������������ȷ����
��� | ������ | ��ԭ�� | ������Ӧ�� | �������� | ��ԭ���� |
�� | Cl2 | FeBr2 | / | Fe3+ Br2 | Cl�� |
�� | KClO3 | Ũ���� | / | Cl2 | |
�� | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A�����Т���ķ�Ӧ������һ�ֻ�����Ԫ�ر�����
B��������ǿ���ıȽϣ� KClO3��Fe3+��Cl2��Br2
C�����Т��鷴Ӧ�Ļ�ԭ������KCl������ת����Ŀ��6e��
D�����Т��鷴Ӧ�����ӷ���ʽΪ��2MnO4��+ 3H2O2 + 6H+=2Mn2+ + 4O2��+ 6H2O
 O2��g����FeO��s�� ��H����272.0kJ?mol-1
O2��g����FeO��s�� ��H����272.0kJ?mol-1 O2��g����Al2O3��s�� ��H����1675.7kJ?mol-1
O2��g����Al2O3��s�� ��H����1675.7kJ?mol-1
 Na2S��s��+4H2O��g�����÷�Ӧ��ƽ�ⳣ������ʽΪ ����֪K1000�� < K1200��, ��������ϵ�¶�,��������ƽ����Է��������� (���������С�����䡱)��
Na2S��s��+4H2O��g�����÷�Ӧ��ƽ�ⳣ������ʽΪ ����֪K1000�� < K1200��, ��������ϵ�¶�,��������ƽ����Է��������� (���������С�����䡱)��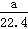 NA
NA