题目内容
15.CH4是天然气的主要成分,其电子式为 ;燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;其燃烧含碳产物的结构式为:O=C=O;CH4与Cl2生成CCl4的化学方程式CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.
;燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;其燃烧含碳产物的结构式为:O=C=O;CH4与Cl2生成CCl4的化学方程式CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.
分析 1个甲烷分子中含1个C、4个H原子,存在4个C-H键,为正四面体结构;甲烷在氧气充分燃烧生成二氧化碳和水;二氧化碳中存在2个C=O键,甲烷与氯气发生取代反应生成四氯化碳和氯化氢,据此解答.
解答 解:1个甲烷分子中含1个C、4个H原子,存在4个C-H键,为正四面体结构,电子式:;甲烷在氧气充分燃烧生成二氧化碳和水,方程式:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
二氧化碳中存在2个C=O键,结构式为:O=C=O; 甲烷与氯气发生取代反应生成四氯化碳和氯化氢,方程式:CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl;
故答案为: ;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O;O=C=O; CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.
;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O;O=C=O; CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.
点评 本题考查了甲烷的结构及性质,明确甲烷碳为饱和碳原子结构特点是解题关键,注意烷烃都是饱和烃,特征反应为取代反应,题目难度不大.

练习册系列答案
相关题目
6.下列物质中,只含离子键的是( )
| A. | O2 | B. | KOH | C. | MgO | D. | CO2 |
10.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
由此可判断这四种金属的活动性顺序是( )
| 实验装置 | 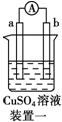 | 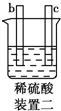 | 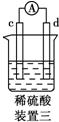 |  |
| 部分实验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
| A. | a>b>c>d | B. | b>c>d>a | C. | d>a>b>c | D. | a>b>d>c |
7.在钠与水反应的实验操作中,符合化学实验安全规则的是( )
| A. | 不经切割,直接用大块的钠做实验 | B. | 用手小心抓住钠块投入烧杯中 | ||
| C. | 在烧杯口盖上玻片后再观察现象 | D. | 将剩余的钠块放入废液缸 |
5.下列属于氧化物的是( )
| A. | 冰水混合物 | B. | 氧气 | C. | 氯酸钾 | D. | 乙醇 |