题目内容
3.常温下,饱和NaClO溶液的pH约为11.某消毒液的主要成分为NaClO,洁厕灵主要成分为HCl.下列解释相关事实的离子方程式中不合理的是( )| A. | 该消毒液加白醋生成HClO,可增强消毒能力:H++ClO-═HClO | |
| B. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-═ClO-+Cl-+H2O | |
| C. | 常温下,该消毒液的pH≈11,是因为:ClO-+H2O?HClO+OH- | |
| D. | 该消毒液与洁厕灵混用会引起中毒:2H++Cl-+ClO-═Cl2↑+H2O |
分析 A.醋酸在离子反应中保留化学式;
B.氯气与NaOH反应生成氯化钠、次氯酸钠和水,遵循电子、电荷守恒;
C.该消毒液的pH≈11,水解显碱性;
D.消毒液与洁厕灵混用,发生氧化还原反应生成氯气.
解答 解:A.醋酸在离子反应中保留化学式,离子反应为CH3COOH+ClO-═CH3COO-+HClO,故A错误;
B.氯气与NaOH反应生成氯化钠、次氯酸钠和水,离子反应为Cl2+2OH-═ClO-+Cl-+H2O,遵循电子、电荷守恒,故B正确;
C.该消毒液的pH≈11,水解显碱性,水解离子反应为ClO-+H2O?HClO+OH-,故C正确;
D.消毒液与洁厕灵混用,发生氧化还原反应生成氯气,离子反应为2H++Cl-+ClO-═Cl2↑+H2O,故D正确;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意水解、氧化还原反应的应用,题目难度不大.

练习册系列答案
相关题目
11.下列化学用语书写正确的是( )
| A. | 丙酸的结构简式:CH3CH2COOH | B. | 甲烷的结构式:CH4 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙醇的结构式: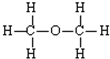 |
18.下列各组物质中属于同分异构体的是( )
| A. |  和 和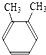 | B. | CH3CH2OH和CH3 CH2-O-CH2CH3 | ||
| C. | 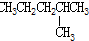 和 和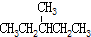 | D. | 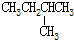 和 和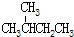 |
8.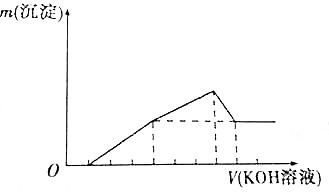 把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
 把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )| A. | 1:1 | B. | 8:9 | C. | 2:3 | D. | 4:3 |
15.下列各组物质互为同分异构体的是( )
| A. | CH3CH2CH3 和 CH3CH(CH3)CH3 | B. |  和 和  | ||
| C. | CH3COOCH2CH3和CH3COOH | D. | CH3CH2CHO和CH3CH2CH2OH |
12.用溶质质量分数为98%的浓硫酸和溶质质量分数为18%的稀硫酸配制500g溶质质量分数为28%的硫酸,需要浓硫酸和稀硫的质量分别为( )
| A. | 62.5g 437.5g | B. | 71.4g 428.6g | ||
| C. | 437.5g 62.5g | D. | 428.6g 71.4g |
15.下列化合物中含有手性碳原子的是( )
| A. | CCl2F2 | B. | CH3-CHCl-COOH | C. | CH3CH2OH | D. | CH2Cl-OH |