题目内容
20.某校化学兴趣小组同学取锌粒与浓H2SO4充分反应制取SO2气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)准备做实验,但是老师说收集到的气体(X)可能含有杂质.(1)该化学兴趣小组制得的气体(X)中混有的主要杂质气体可能是H2(填化学式),写出此过程所发生的2个化学反应方程式:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4 +SO2↑+2H2O、Zn+2H2SO4=ZnSO4 +H2↑.
(2)一定质量的Zn与87.5mL 16.0mol/L浓硫酸充分反应,反应后称量剩余锌发现质量减少了78g,产生SO2体积(标准状况下)=4.48L.
(3)为证实相关分析,该小组的同学设计了如图1所示的实验装置,对此气体(X)取样进行认真研究(遇有气体吸收过程,可视为全吸收).

①酸性KMnO4溶液的作用是除去二氧化硫气体;B中添加的试剂是浓硫酸.
②装置C中所装药品为CuO,可证实气体X中混有较多量某杂质气体的实验现象是C中黑色粉末变为红色,D中的白色固体变为蓝色.
(4)实验室中某些气体的制取、收集及尾气处理装置如图2所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是D
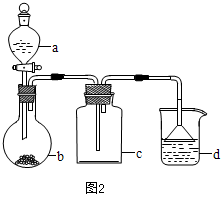
| 选项 | a物质 | b物质 | c收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
分析 (1)浓硫酸随反应进行浓度变小后,稀硫酸和锌反应生成氢气,所以气体杂质含有氢气;锌和浓硫酸反应生成硫酸锌,二氧化硫和水,锌和稀硫酸反应生成硫酸锌和氢气,据此书写化学方程式;
(2)硫酸完全反应,发生反应:Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,Zn+H2SO4=ZnSO4+H2↑,结合方程式计算;
(3)证明气体中含有氢气,酸性高锰酸钾溶液目的吸收生成的二氧化硫气体,则B装置中加浓硫酸吸收气体表面的水分,装置C将残留的气体通过灼热的氧化铜反应,目的是验证该气体具有还原性,装置D无水硫酸铜检验水,若变蓝色则C装置反应生成水,根据元素守恒且该气体具有还原性,则X气体为H2,据此进行分析;
(4)A.氨气密度比空气小;
B.澄清石灰水浓度较小;
C.铁与稀硝酸反应产生的气体为NO,一氧化氮难溶于水;
D.浓盐酸和高锰酸钾反应生成氯气.
解答 解:(1)浓硫酸随反应进行浓度变小后,稀硫酸和锌反应生成氢气,所以气体杂质含有氢气;锌和浓硫酸反应生成硫酸锌,二氧化硫和水,故对应的化学方程式为Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4 +SO2↑+2H2O,锌和稀硫酸反应生成硫酸锌和氢气,
故对应的化学方程式为Zn+2H2SO4=ZnSO4 +H2↑,
故答案为:H2;Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4 +SO2↑+2H2O、Zn+2H2SO4=ZnSO4 +H2↑;
(2)一定质量的Zn与87.5mL 16.0mol/L的H2SO4的浓溶液充分反应,反应后称量剩余锌发现质量减少了78.0g,则参加反应Zn的物质的量为1.2mol,H2SO4的物质的量为0.0875L×16mol/L=1.4mol,
由于硫酸都没有剩余,设与浓硫酸反应的Zn为xmol,与稀硫酸反应的Zn为ymol,则:
Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O
x 2x x x
Zn+H2SO4=ZnSO4+H2↑
y y y
由题意可知:
$\left\{\begin{array}{l}{x+y=1.2}\\{2x+y=1.4}\end{array}\right.$,解得x=0.2,y=1.0,
产生SO2体积(标准状况下)=0.2mol×22.4L/mol=4.48L,
故答案为:4.48;
(3)证明气体中含有氢气,酸性高锰酸钾溶液目的吸收生成的二氧化硫气体,则B装置中加浓硫酸吸收气体表面的水分,装置C将残留的气体通过灼热的氧化铜反应,目的是验证该气体具有还原性,装置D无水硫酸铜检验水,若变蓝色则C装置反应生成水,根据元素守恒且该气体具有还原性,则X气体为H2,
①由以上分析得,酸性KMnO4溶液的作用是除去二氧化硫气体;B中添加的试剂是浓硫酸,
故答案为:除去二氧化硫气体;浓硫酸;
②由以上分析得,装置C中所装药品为CuO;可证实气体X中混有较多量某杂质气体的实验现象是C中黑色粉末变为红色,D中的白色固体变为蓝色,
故答案为:CuO;C中黑色粉末变为红色,D中的白色固体变为蓝色;
(4)A.氨气密度比空气小,集气瓶中导管应短进长出,故A错误;
B.澄清石灰水浓度较小,不能用来处理尾气,故B错误;
C.铁与稀硝酸反应产生的气体为NO,一氧化氮难溶于水,不能用溶液吸收,故C错误;
D.浓盐酸和高锰酸钾反应生成氯气,氯气可用氢氧化钠吸收,故D正确;
故答案为:D.
点评 本题考查了制备方案设计,题目难度中等,侧重于考查学生的实验探究能力,注意把握硫酸及其化合物的性质,明确实验目的和实验原理是解题的关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案①CH3-CH═CH2和CH2═CH2的最简式相同
②CH≡CH和C6H6含碳量相同
③丁二烯和丁烯为同分异构体
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2L的戊烷所含的分子数为0.5NA(NA为阿伏加德罗常数)
⑥石油的催化重整和煤的干馏均可以得到芳香烃,说明石油和煤中含有芳香烃.
| A. | ①②⑥ | B. | ②③④ | C. | ②④⑥ | D. | ③⑤⑥ |
①向溶液中加入过量(NH4)2CO3,得到气体甲、溶液甲和白色沉淀甲;
②向溶液甲中加入过量Ba(OH)2,加热得到气体乙、溶液乙和白色沉淀乙;
③向溶液乙中加入Cu粉和过量稀硫酸,得到气体丙、溶液丙和白色沉淀丙.
下列说法正确的是( )
| A. | 该粉末中可能是Fe2(SO4)3和Al(NO3)3的混合物 | |
| B. | 沉淀乙和丙都是BaSO4 | |
| C. | 气体乙和丙分别是NH3和H2 | |
| D. | 气体甲可能由A13+与CO32-相互促进水解得到 |
| A. | 寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量 | |
| B. | 寻找优质催化剂,在常温常压下使CO2分解生成碳与O2 | |
| C. | 寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2) | |
| D. | 将固态碳合成为C60,以C60作为燃料 |

| A. | 图甲中,为检查装置的气密性,可关闭分液漏斗A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否复原 | |
| B. | 图已中,可以比较KMnO4、Cl2和S氧化性的相对强弱 | |
| C. | 将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升 | |
| D. | 图丁中,可用装置验证NaHCO3和Na2CO3的热稳定性强弱 |
| A. | 某无色透明的酸性溶液:Cl-、Na+、MnO4-、SO42- | |
| B. | 含CO32-的溶液:K+、Na+、AlO2-、Cl- | |
| C. | 能使pH试纸变深蓝色的溶液:Na+、NH4+、K+、CO32- | |
| D. | 由水电离产生的c(H+)=10-12mol/L的溶液:K+、I-、Cl-、NO3- |

| A. | 装置①:制取乙炔并验证炔烃的性质 | |
| B. | 装置②:检验乙醇的还原性,溶液颜色从紫红色色变无色 | |
| C. | 装置③:产生银镜,说明蔗糖分子中含有醛基官能团 | |
| D. | 装置④:酸性KMnO4溶液中出现气泡且逐渐褪色,说明有不同于烷烃的另一类烃产生 |
| A. | 苯甲醇 | B. | 环己醇 | C. | 1-己醇 | D. | 间甲基苯甲醇 |