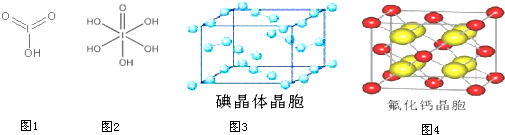
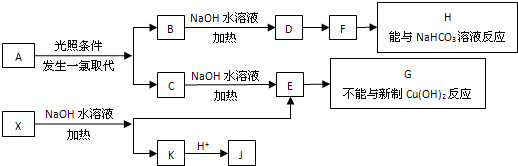
题目内容
已知A、B、C、D四种物质中均含同种元素,且它们之间的转化关系如图.下列说法正确的是( )
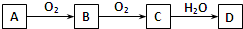
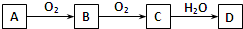
| A、A一定为单质 |
| B、C一定为氧化物 |
| C、D一定为酸 |
| D、A、B、C的相对分子质量之差为16或16的倍数 |
考点:无机物的推断
专题:
分析:A、B、C、D四种物质中均含同种元素,A能连续被氧化生成C,说明B中有变价元素,A可能是非金属元素单质,如:C、S、N,也可能是金属单质,如Na,也可能是化合物如NH3,根据物质之间的转化分析解答.
解答:
解:A、A可以为化合物NH3,NH3
NO
NO2
HNO3,故A错误;
B、B被氧气氧化生成氧化物C,所以C是氧化物,故B正确;
C、如果C是Na,Na
Na2O
Na2O2
NaOH,则D是NaOH,故C错误;
D、A、B、C、D相对分子质量之差不一定为16或16的倍数,如NH3
NO,故D错误.
故选:B.
| O2 |
| O2 |
| H2O |
B、B被氧气氧化生成氧化物C,所以C是氧化物,故B正确;
C、如果C是Na,Na
| O2 |
| O2 |
| H2O |
D、A、B、C、D相对分子质量之差不一定为16或16的倍数,如NH3
| O2 |
故选:B.
点评:本题考查了无机物的推断,短周期中能实现上述关系的主要有Na、C、S、N元素的单质、化合物,同时考查学生发散思维能力、归纳总结能力,难度中等.

练习册系列答案
相关题目
 常温下,在0.1mol?L-1KAl(SO4)2溶液中,加入KOH固体,如图,横坐标
常温下,在0.1mol?L-1KAl(SO4)2溶液中,加入KOH固体,如图,横坐标为溶液的pH,纵坐标为Al3+离子或AlO2-离子的物质的量浓度.(假设Al3+
离子浓度为10-5mol?L-1时,Al3+离子已沉淀完全),下列说法不正确的是( )
| A、从图中数据计算可得Al(OH)3的溶度积Ksp=10-23 |
| B、沉淀Al3+可以控制溶液pH的范围为5~8 |
| C、向KAl(SO4)2溶液中加入KOH固体至pH=7时,c(K+):c(SO42-)=2:1 |
| D、往KAl(SO4)2溶液中加入足量的氢氧化钾溶液,反应的离子方程式可表示为:Al3++4OH-=AlO2-+2H2O |
下列与有机物相关的说法错误的是( )
| A、用溴水可以鉴别乙醇、苯和四氯化碳 |
| B、乙酸乙酯中的少量乙酸可以用氢氧化钠溶液除去 |
| C、用新制氢氧化铜悬浊液可以检验尿液中是否含有葡萄糖 |
| D、用酸性高锰酸钾溶液可以区分乙烷和乙烯 |
25℃时,下列两溶液混合后所得溶液pH<7的是( )
| A、pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
| B、pH=3的盐酸和pH=11的氨水等体积混合 |
| C、pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
| D、pH=3的硫酸和pH=11的氨水等体积混合 |
下列有机物的系统名称中,正确的是( )
| A、2,4,4-三甲基戊烷 |
| B、4-甲基-2-戊烯 |
| C、3-甲基-5-异丙基庚烷 |
| D、1,2,4-三甲基丁烷 |
下列离子方程式正确的是( )
| A、NH4HCO3溶液中加入少量稀NaOH溶液:NH4++OH-=NH3?H2O |
| B、FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C、硫酸亚铁溶液中加入用硫酸酸化的双氧水Fe2++2H++H2O2=Fe3++2H2O |
| D、在通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |
下列有关钠与氯气的反应的叙述,正确的是( )
| A、钠在氯气中剧烈燃烧,生成黑烟 | ||||
| B、钠熔化成小球,与氯气缓慢反应,有蓝色火焰 | ||||
C、该反应的化学方程式为:Na+Cl
| ||||
| D、反应后,钠原子失去电子变成钠离子,氯原子得到电子变成氯离子 |