题目内容
下列离子方程式正确的是( )
| A、NH4HCO3溶液中加入少量稀NaOH溶液:NH4++OH-=NH3?H2O |
| B、FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C、硫酸亚铁溶液中加入用硫酸酸化的双氧水Fe2++2H++H2O2=Fe3++2H2O |
| D、在通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.少量NaOH,先与碳酸氢根离子反应;
B.足量的氯气,亚铁离子、溴离子均被氧化;
C.电子、电荷不守恒;
D.加足量的溴水,发生氧化还原反应生成硫酸钠.
B.足量的氯气,亚铁离子、溴离子均被氧化;
C.电子、电荷不守恒;
D.加足量的溴水,发生氧化还原反应生成硫酸钠.
解答:
解:A.NH4HCO3溶液中加入少量稀NaOH溶液的离子反应为HCO3-+OH-=CO32-+H2O,故A错误;
B.FeBr2溶液中通入足量的氯气的离子反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故B错误;
C.硫酸亚铁溶液中加入用硫酸酸化的双氧水的离子反应为2Fe2++2H++H2O2=2Fe3++2H2O,故C错误;
D.通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解)的离子反应为HSO3-+Br2+H2O=3H++2Br-+SO42-,故D正确;
故选D.
B.FeBr2溶液中通入足量的氯气的离子反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故B错误;
C.硫酸亚铁溶液中加入用硫酸酸化的双氧水的离子反应为2Fe2++2H++H2O2=2Fe3++2H2O,故C错误;
D.通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解)的离子反应为HSO3-+Br2+H2O=3H++2Br-+SO42-,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
今有五种有机物:其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是( )
①CH2OH(CHOH)4CHO ②CH3(CH2)3OH③CH2═CH-CH2OH ④CH2═CH-COOCH3⑤CH2═CH-COOH.
①CH2OH(CHOH)4CHO ②CH3(CH2)3OH③CH2═CH-CH2OH ④CH2═CH-COOCH3⑤CH2═CH-COOH.
| A、③⑤ | B、①②⑤ | C、②④ | D、③④ |
已知A、B、C、D四种物质中均含同种元素,且它们之间的转化关系如图.下列说法正确的是( )
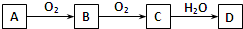
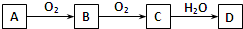
| A、A一定为单质 |
| B、C一定为氧化物 |
| C、D一定为酸 |
| D、A、B、C的相对分子质量之差为16或16的倍数 |
已知酸性: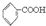 >H2CO3>
>H2CO3> >HCO3-将
>HCO3-将 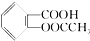 转变为
转变为 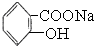 ,可行的方法是( )
,可行的方法是( )
 >H2CO3>
>H2CO3> >HCO3-将
>HCO3-将  转变为
转变为  ,可行的方法是( )
,可行的方法是( )| A、向该溶液中加入足量的稀硫酸,加热 |
| B、将该物质与稀硫酸共热后,再加入足量的NaOH溶液 |
| C、将该物质与足量的NaOH溶液共热,再通入足量CO2气体 |
| D、将该物质与稀硫酸共热后,再加入足量的NaHCO3溶液 |
已知I2+SO32-+H2O═SO42-+2I-+2H+.某无色溶液中只可能含有I-,NH4+,Ba2+,SO32-,MnO4-中的一种或几种,若向该溶液中滴加少量的溴水,溶液仍为无色,下列判断正确的是( )
| A、该溶液中肯定不含I- |
| B、该溶液中可能含有Ba2+ |
| C、该溶液中肯定含有NH4+ |
| D、该溶液中可能含有MnO4- |
下列说法不正确的是( )
| A、大量使用的不是纯金属而是它们的合金 |
| B、目前已制得的纯金属只有90多种,但制得的合金已达几千种 |
| C、钢是最纯的铁 |
| D、废弃铝质包装既浪费金属材料又造成环境污染 |