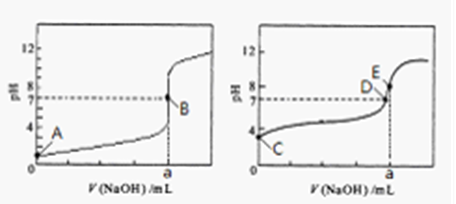
题目内容
下列叙述不正确的是( )
| A.PH相等体积相等的盐酸和醋酸加水稀释10倍后,前者的PH大于后者 |
| B.PH相等体积相等的盐酸和醋酸分别中和0.1mol/L的NaOH溶液,消耗NaOH溶液体积相等 |
| C.等浓度等体积的盐酸和醋酸与足量的锌粉反应,开始时前者产生H2的速率大于后者,最终产生的H2相等。 |
| D.等浓度等体积的盐酸和醋酸分别中和0.1mol/L的NaOH溶液,消耗NaOH溶液体积相等 |
B
醋酸是弱电解质,存在电离平衡,稀释促进电离,所以pH相等体积相等的盐酸和醋酸加水稀释10倍后,前者的酸性弱于后者,A正确。pH相等的盐酸和醋酸,后者的浓度大于前者,所以后者消耗的氢氧化钠等于前者,B不正确。等浓度的盐酸和醋酸中,前者溶液中氢离子大于后者,所以起始时,反应速率是相同的。但由于二者的体积和浓度都相等,所以最终生成的氢气是相等的,C正确。同样选项D也是正确的,所以答案选B。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
 CH3COO-+ H+,对于该平衡,下列叙述正确的是( )
CH3COO-+ H+,对于该平衡,下列叙述正确的是( ) NH4++NH2-,两种离子的平衡浓度均为1×10-15mol/L,下列有关叙述不正确的是
NH4++NH2-,两种离子的平衡浓度均为1×10-15mol/L,下列有关叙述不正确的是