题目内容
在某固定容积的密闭容器中,进行下列反应:C(s)+H2O(g)?CO(g)+H2(g)
(1)未达平衡前,增加炭的量,υ正 (填“增大”、“减小”或“不变”,下同);减小c(H2),υ逆 .
(2)达到平衡后,增加炭的量,K (填“增大”、“减小”或“不变”,下同);减小c(H2),K .试写出影响K 的因素 .
(3)在某固定容积的密闭容器中进行的反应:CO(g)+H2O(g)?CO2(g)+H2(g)
若提高c(H2O),则其自身的转化率 (填“增大”、“减小”或“不变”,下同),CO的转化率 ,c(H2O) .
(1)未达平衡前,增加炭的量,υ正
(2)达到平衡后,增加炭的量,K
(3)在某固定容积的密闭容器中进行的反应:CO(g)+H2O(g)?CO2(g)+H2(g)
若提高c(H2O),则其自身的转化率
考点:化学平衡的影响因素,化学反应速率的影响因素
专题:
分析:(1)炭是固态,增大炭的量不影响反应速率;减小生成物的浓度,逆反应速率迅速减小;
(2)K指受温度影响;
(3)提高c(H2O),平衡正向移动,CO转化率增大,水蒸气转化率减小,据此分析.
(2)K指受温度影响;
(3)提高c(H2O),平衡正向移动,CO转化率增大,水蒸气转化率减小,据此分析.
解答:
解:(1)炭是固态,增大炭的量不影响反应速率;减小生成物的浓度,逆反应速率迅速减小,故答案为:不变;减小;
(2)K只受温度影响,不受浓度.压强的影响,故答案为:不变;不变;温度;
(3)提高水蒸气的浓度,平衡正向移动,CO的转化率增大,水蒸气的转化率减小,故答案为:减小;增大;减小.
(2)K只受温度影响,不受浓度.压强的影响,故答案为:不变;不变;温度;
(3)提高水蒸气的浓度,平衡正向移动,CO的转化率增大,水蒸气的转化率减小,故答案为:减小;增大;减小.
点评:本题考查了影响化学反应速率和影响平衡移动的因素,题目难度中等.

练习册系列答案
相关题目
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法 |
已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11.下列说法正确的是( )
| A、25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B、25℃时,Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C、25℃时,Mg(OH)2固体在20 mL 0.01 mol?L-1氨水中的Ksp比在20 mL 0.01 mol?L-1NH4Cl溶液中的Ksp小 |
| D、25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
下列食品添加剂与其作用不相匹配的是( )
| A、叶绿素:着色剂 |
| B、亚硝酸钠:调味剂 |
| C、碳酸钠:疏松剂 |
| D、苯甲酸钠:防腐剂 |
氢氟酸是一种弱酸,具有强烈的腐蚀性.常温下,在氢氟酸加水稀释的过程中
的变化趋势是( )
| c(H+) |
| c(F-) |
| A、变大 | B、变小 |
| C、不变 | D、无法确定 |
下列实验过程正确的是( )
| A、用酒精萃取碘水中的碘 |
| B、用稀硫酸清洗做焰色反应的铂丝 |
| C、用加热法分离氯化钠和碳酸钙的固体混合物 |
| D、分液操作时分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol?L-1?min-1 |
| B、v(B)=0.01 mol?L-1?s-1 |
| C、v(C)=0.8 mol?L-1?min-1 |
| D、v(D)=1 mol?L-1?min-1 |
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如表所示.已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是( )
| X | ||||
| Y | Z | W |
| A、原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
| B、Z的最高价氧化物的水化物酸性比W的强 |
| C、X的简单气态氢化物的稳定性比W的弱 |
| D、X分别与Y、Z形成的化合物中化学键类型相同 |
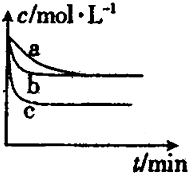 1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:
1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题: