题目内容
21世纪是钛的世纪.如图1是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
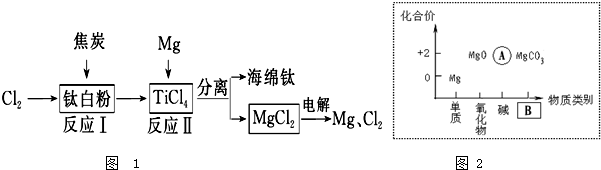
(1)反应Ⅰ在800~900℃的条件下进行,还生成一种可燃性无色气体,该反应的化学方程式为 ;
(2)回答下列问题;
①如图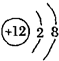 为镁元素的某种粒子结构示意图,该图表示(填序号) .
为镁元素的某种粒子结构示意图,该图表示(填序号) .
A.分子 B.原子 C.阳离子 D.阴离子
镁原子在化学反应中容易失去电子,镁是一种(填“活泼”或“不活泼”) 金属.除了能与氧气反应,还可以与氮气,二氧化碳等反应.
②已知氮化镁中氮元素的化合价为-3价,氮化镁的化学式为 .
③以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.
如图2为镁的价类图,请分析该图后填写:
A处的化学式为: ,B处的物质类别是: .
(3)反应Ⅱ可获得海锦钛,化学方程式表示为TiCl4+2Mg
Ti+2MgCl2.该反应在下列哪种环境中进行 (填序号).
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
(4)该工艺流程中,可以循环使用的物质有 .
(5)反应Ⅱ可通过如下反应制得,TiCl4+2Mg
Ti+2MgCl2.若要制得24g钛,需要镁的质量是多少克?(写出计算过程) .

(1)反应Ⅰ在800~900℃的条件下进行,还生成一种可燃性无色气体,该反应的化学方程式为
(2)回答下列问题;
①如图
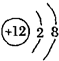 为镁元素的某种粒子结构示意图,该图表示(填序号)
为镁元素的某种粒子结构示意图,该图表示(填序号)A.分子 B.原子 C.阳离子 D.阴离子
镁原子在化学反应中容易失去电子,镁是一种(填“活泼”或“不活泼”)
②已知氮化镁中氮元素的化合价为-3价,氮化镁的化学式为
③以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.
如图2为镁的价类图,请分析该图后填写:
A处的化学式为:
(3)反应Ⅱ可获得海锦钛,化学方程式表示为TiCl4+2Mg
| ||
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
(4)该工艺流程中,可以循环使用的物质有
(5)反应Ⅱ可通过如下反应制得,TiCl4+2Mg
| ||
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:由流程可知氯气、焦炭以及钛白粉反应生成TiCl4,加入镁粉生成海绵钛,分离后得到氯化镁电解可用于冶炼镁,
(1)反应Ⅰ在800~900℃的条件下进行,还生成一种可燃性无色气体,应为CO,同时生成TiCl4;
(2)①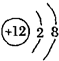 为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子;
为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子;
②根据化合价代数和为0的原则判断;
③A为碱,B为盐;
(3)从镁易与氧气、二氧化碳以及氮气反应的角度判断;
(4)电解氯化镁生成镁和氯气,可循环使用;
(5)根据方程式列式计算.
(1)反应Ⅰ在800~900℃的条件下进行,还生成一种可燃性无色气体,应为CO,同时生成TiCl4;
(2)①
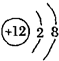 为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子;
为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子;②根据化合价代数和为0的原则判断;
③A为碱,B为盐;
(3)从镁易与氧气、二氧化碳以及氮气反应的角度判断;
(4)电解氯化镁生成镁和氯气,可循环使用;
(5)根据方程式列式计算.
解答:
解:由流程可知氯气、焦炭以及钛白粉反应生成TiCl4,加入镁粉生成海绵钛,分离后得到氯化镁电解可用于冶炼镁,
(1)反应Ⅰ在800~900℃的条件下进行,还生成一种可燃性无色气体,应为CO,同时生成TiCl4,方程式为Cl2+TiO2+C
TiCl4+CO,
故答案为:Cl2+TiO2+C
TiCl4+CO;
(2)①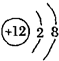 为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子,故答案为:C;活泼;
为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子,故答案为:C;活泼;
②已知氮化镁中氮元素的化合价为-3价,镁为+2价,则氮化镁的化学式为Mg3N2,故答案为:Mg3N2;
③由图象可知A为碱,即Mg(OH)2,B为盐,故答案为:Mg(OH)2;盐;
(3)镁易与氧气、二氧化碳以及氮气反应,应在惰性气体中反应,故答案为:A;
(4)电解氯化镁生成镁和氯气,可循环使用,故答案为:Mg、Cl2;
(5)TiCl4+2Mg
Ti+2MgCl2.
48 48
m 24g
m=24g,
故答案为:24g.
(1)反应Ⅰ在800~900℃的条件下进行,还生成一种可燃性无色气体,应为CO,同时生成TiCl4,方程式为Cl2+TiO2+C
| ||
故答案为:Cl2+TiO2+C
| ||
(2)①
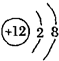 为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子,故答案为:C;活泼;
为镁离子的结构示意图,说明镁是一种活泼金属,易失去电子,故答案为:C;活泼;②已知氮化镁中氮元素的化合价为-3价,镁为+2价,则氮化镁的化学式为Mg3N2,故答案为:Mg3N2;
③由图象可知A为碱,即Mg(OH)2,B为盐,故答案为:Mg(OH)2;盐;
(3)镁易与氧气、二氧化碳以及氮气反应,应在惰性气体中反应,故答案为:A;
(4)电解氯化镁生成镁和氯气,可循环使用,故答案为:Mg、Cl2;
(5)TiCl4+2Mg
| ||
48 48
m 24g
m=24g,
故答案为:24g.
点评:本题综合考查物质的分离、提纯,为高频考点,侧重学生的分析能力和实验能力的考查,注意把握反应的流程以及相关物质的性质,难度不大.

练习册系列答案
相关题目
 如图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是( )
如图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是( )| A、B中收集到的气体是氢气 |
| B、烧杯中双氧水溶液作用是将Fe2+还原为Fe3+ |
| C、A中的氧化铁与盐酸反应生成氯化铁 |
| D、烧杯中溶液在氯化氢气氛下,蒸发浓缩、冷却结晶、过滤后得到氯化铁晶体 |
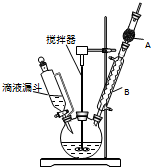 三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
 选用滴定管
选用滴定管
 是有机物A的同分异构体,下列说法错误的是
是有机物A的同分异构体,下列说法错误的是 实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)?NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵.
实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)?NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵.
 与CH3CHO两者之间能发生类似①、②的两步反应,则生成有机物的结构简式为
与CH3CHO两者之间能发生类似①、②的两步反应,则生成有机物的结构简式为