ЬтФПФкШн
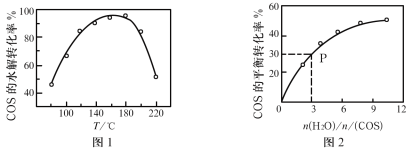
ЁОЬтФПЁПМзДМЪЧживЊЕФЛЏЙЄдСЯЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЁЃдкЬхЛ§ПЩБфЕФУмБеШнЦїжаЭЖШы0.5molCOКЭ1molH2ЃЌВЛЭЌЬѕМўЯТЗЂЩњЗДгІЃКCO(g)+2H2(g)![]() CH3OH(g)ЁЃЪЕбщВтЕУЦНКтЪБCH3OHЕФЮяжЪЕФСПЫцЮТЖШЁЂбЙЧПЕФБфЛЏШчЭМ1ЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
CH3OH(g)ЁЃЪЕбщВтЕУЦНКтЪБCH3OHЕФЮяжЪЕФСПЫцЮТЖШЁЂбЙЧПЕФБфЛЏШчЭМ1ЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
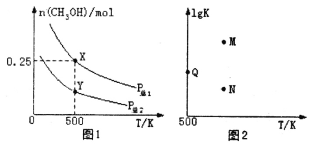
A.Pзм1<Pзм2
B.ЛьКЯЦјЬхЕФУмЖШВЛдйЗЂЩњБфЛЏЃЌЫЕУїИУЗДгІвбДяЕНЦНКтзДЬЌ
C.ЭМ2жаMЕуФме§ШЗБэЪОИУЗДгІЦНКтГЃЪ§ЕФЖдЪ§(1gK)гыЮТЖШЕФЙиЯЕ
D.ШєPзм1=0.25MPaЃЌдђYЕуЕФЦНКтГЃЪ§Kp=64(MPa)-2
ЁОД№АИЁПBD
ЁОНтЮіЁП
AЃЎЖдгкЗДгІCOЃЈgЃЉ+2H2ЃЈgЃЉ![]() CH3OHЃЈgЃЉЃЌдіДѓбЙЧПЃЌЦНКте§ЯђвЦЖЏЃЌМзДМЕФЮяжЪЕФСПдіДѓЃЛ
CH3OHЃЈgЃЉЃЌдіДѓбЙЧПЃЌЦНКте§ЯђвЦЖЏЃЌМзДМЕФЮяжЪЕФСПдіДѓЃЛ
BЃЎШнЦїЬхЛ§ПЩБфЃЌЦНКтЪБЃЌШнЦїЬхЛ§ВЛБфЃЌУмЖШВЛБфЃЛ
CЃЎЩ§ИпЮТЖШМзДМЕФЮяжЪЕФСПМѕЩйЃЌЫЕУїЩ§ИпЮТЖШЃЌЦНКтФцЯђвЦЖЏЃЛ
DЃЎXЁЂYЕудкЯрЭЌЮТЖШЯТЃЌдђЦНКтГЃЪ§ЯрЭЌЃЌXЕуМзДМЕФЮяжЪЕФСПЮЊ0.25molЃЌПЩМЦЫуЦНКтЪБИїЮяжЪЕФСПЃЌНјЖјМЦЫуЗжбЙЃЌНсКЯЗжбЙМЦЫуЦНКтГЃЪ§ЁЃ
AЃЎЖдгкЗДгІCOЃЈgЃЉ+2H2ЃЈgЃЉ![]() CH3OHЃЈgЃЉЃЌдіДѓбЙЧПЃЌЦНКте§ЯђвЦЖЏЃЌМзДМЕФЮяжЪЕФСПдіДѓЃЌгЩЭМЯѓПЩжЊPзм1ЃОPзм2ЃЌЙЪAДэЮѓЃЛ
CH3OHЃЈgЃЉЃЌдіДѓбЙЧПЃЌЦНКте§ЯђвЦЖЏЃЌМзДМЕФЮяжЪЕФСПдіДѓЃЌгЩЭМЯѓПЩжЊPзм1ЃОPзм2ЃЌЙЪAДэЮѓЃЛ
BЃЎШнЦїЬхЛ§ПЩБфЃЌДяЕНЦНКтЪБЃЌШнЦїЬхЛ§ВЛБфЃЌгЩгкЦјЬхЕФжЪСПВЛБфЃЌдђУмЖШВЛБфЃЌПЩЫЕУїДяЕНЦНКтзДЬЌЃЌЙЪBе§ШЗЃЛ
CЃЎЩ§ИпЮТЖШМзДМЕФЮяжЪЕФСПМѕЩйЃЌЫЕУїЩ§ИпЮТЖШЃЌЦНКтФцЯђвЦЖЏЃЌдђЩ§ИпЮТЖШЃЌlgKМѕаЁЃЌNЕуФме§ШЗБэЪОИУЗДгІЦНКтГЃЪ§ЕФЖдЪ§ЃЈ1gKЃЉгыЮТЖШЕФЙиЯЕЃЌЙЪCДэЮѓЃЛ
DЃЎXЁЂYЕудкЯрЭЌЮТЖШЯТЃЌдђЦНКтГЃЪ§ЯрЭЌЃЌXЕуМзДМЕФЮяжЪЕФСПЮЊ0.25molЃЌдђ

дђKЃЈYЃЉ=KЃЈXЃЉ=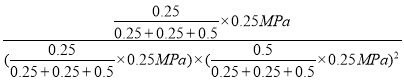 =64ЃЈMPaЃЉ-2ЃЌЙЪDе§ШЗЁЃ
=64ЃЈMPaЃЉ-2ЃЌЙЪDе§ШЗЁЃ
ЙЪбЁЃКBDЁЃ

ЁОЬтФПЁПЪЕбщЪвПЩгУвчСїЗЈСЌајжЦБИЮоЫЎЫФТШЛЏЮ§ЃЈSnCl4ЃЉЁЃSnCl4взЛгЗЂЃЌМЋвзЗЂЩњЫЎНтЃЌCl2МЋвзШмгкSnCl4ЁЃжЦБИдРэгыЪЕбщзАжУЭМШчЯТЃК
Sn(s)+2Cl2(g)=SnCl4(l) ІЄH = ЈC511kJmolЃ1

ПЩФмгУЕНЕФгаЙиЪ§ОнШчЯТЃК
ЮяжЪ | Sn | SnCl4 | CuCl2 |
ШлЕу/Ёц | 232 | -33 | 620 |
ЗаЕу/Ёц | 2260 | 114 | 993 |
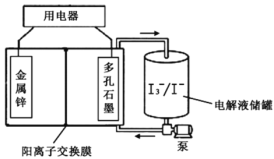
жЦБИЙ§ГЬжаЃЌЮ§СЃж№НЅБЛЯћКФЃЌаыЬсРЯ№НКШћМАЪБЯђЗДгІЦїжаВЙМгЮ§СЃЁЃЕБSnCl4вКУцЩ§жСВрПкИпЖШЪБЃЌвКЬЌВњЮяОВрЙмСїШыНгЪеЦПЁЃЛиД№ЯТСаЮЪЬтЃК
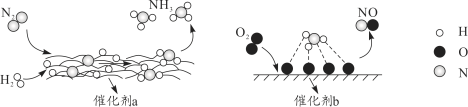
ЃЈ1ЃЉaЙмЕФзїгУЪЧ________ЁЃ
ЃЈ2ЃЉAжаЗДгІЕФРызгЗНГЬЪНЪЧ________ЁЃ
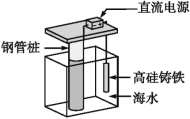
ЃЈ3ЃЉDЕФзїгУЪЧ________ЁЃ
ЃЈ4ЃЉEжаРфШДЫЎЕФзїгУЪЧ________ЁЃ
ЃЈ5ЃЉЮВЦјДІРэЪБЃЌПЩбЁгУЕФзАжУЪЧ________ЃЈЬюађКХЃЉЁЃ

ЃЈ6ЃЉЮ§СЃжаКЌЭдгжЪжТEжаВњЩњCuCl2ЃЌЕЋВЛгАЯьFжаВњЦЗЕФДПЖШЃЌдвђЪЧ________ЁЃ
ЃЈ7ЃЉSnCl4ДжЦЗжаКЌгаCl2ЃЌОЋжЦЪБМгШыЩйаэЮ§аМКѓеєСѓПЩЕУДПОЛЕФSnCl4ЁЃеєСѓЙ§ГЬжаВЛашвЊгУЕНЕФвЧЦїга________ЃЈЬюађКХЃЉЁЃ
AЃЎеєСѓЩеЦП BЃЎЮТЖШМЦ CЃЎНгЪеЦї DЃЎРфФ§Йм EЃЎЮќТЫЦП
ЁОЬтФПЁПCO2ЪЧвЛжжГЃМћЕФЮТЪвЦјЬхЃЌЫќЕФЮќЪеКЭРћгУвВГЩЮЊЯжДњПЦММЕФШШУХПЮЬтЁЃ
(1)КуШнУмБеШнЦїжаЃЌдкCu/ZnOДпЛЏМСзїгУЯТЃЌПЩгУCO2жЦБИМзДМЃКCO2(g) + 3H2(g)CH3OH(g) + H2O(l) ЁїH1ЃЌвбжЊЃК CH3OH(g) +![]() O2(g)=CO2(g) + 2H2O(l) ЁїH2ЃЌаДГіЧтЦјШМЩеШШЕФШШЛЏбЇЗНГЬЪН________(ЁїHгУЁїH1ЁЂ ЁїH2БэЪО)ЁЃФГЮТЖШЯТЃЌдкЬхЛ§ЮЊ2LЕФУмБеШнЦїжаМгШы2mol CO2ЁЂ5mol H2вдМАДпЛЏМСНјааЗДгІЩњГЩCH3OH еєЦјКЭЫЎеєЦјЃЌДяЕНЦНКтЪБH2ЕФзЊЛЏТЪЪЧ60%ЃЌЦфЦНКтГЃЪ§ЮЊ_______ЁЃ
O2(g)=CO2(g) + 2H2O(l) ЁїH2ЃЌаДГіЧтЦјШМЩеШШЕФШШЛЏбЇЗНГЬЪН________(ЁїHгУЁїH1ЁЂ ЁїH2БэЪО)ЁЃФГЮТЖШЯТЃЌдкЬхЛ§ЮЊ2LЕФУмБеШнЦїжаМгШы2mol CO2ЁЂ5mol H2вдМАДпЛЏМСНјааЗДгІЩњГЩCH3OH еєЦјКЭЫЎеєЦјЃЌДяЕНЦНКтЪБH2ЕФзЊЛЏТЪЪЧ60%ЃЌЦфЦНКтГЃЪ§ЮЊ_______ЁЃ
(2)ЙЄвЕЩЯгУCO2ДпЛЏМгЧтжЦШЁЖўМзУбЃК2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)ЁЃдкСНИіЯрЭЌЕФКуШнУмБеШнЦїжаЃЌГфШыЕШСПЕФЗДгІЮяЃЌЗжБ№вдIrКЭCeзїДпЛЏМСЃЌЗДгІНјааЯрЭЌЕФЪБМфКѓВтЕУЕФCO2ЕФзЊЛЏТЪІС(CO2)ЫцЗДгІЮТЖШЕФБфЛЏЧщПіШчЭМЫљЪОЃК
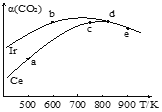
ЂйгУIrКЭCeзїДпЛЏМСЪБЃЌЗДгІЕФЛюЛЏФмИќЕЭЕФЪЧ_________ЃЛ
ЂкaЁЂbЁЂcЁЂdКЭeЮхжжзДЬЌЃЌЗДгІвЛЖЈДяЕНЦНКтзДЬЌЕФЪЧ________ЃЌЗДгІЕФІЄH ____0(ЬюЁАЃОЁБЁЂЁА=ЁБЛђЁАЃМЁБ)ЃЛ
ЂлДгзДЬЌaЕНcЃЌCO2зЊЛЏТЪВЛЖЯдіДѓЕФдвђЪЧ__________ЃЛ
ЂмвбжЊTЁцЯТЃЌНЋ2 molCO2КЭ6 molH2ЭЈШыЕНЬхЛ§ЮЊV LЕФУмБеШнЦїжаНјааЩЯЪіЗДгІЃЌЗДгІЪБМфгыШнЦїФкЕФзмбЙЧПЪ§ОнШчБэЃК
ЪБМфt/min | 0 | 10 | 20 | 30 | 40 |
змбЙЧПp/1000kPa | 1.0 | 0.83 | 0.68 | 0.60 | 0.60 |
ИУЗДгІЦНКтЪБCO2ЕФзЊЛЏТЪЮЊ___________ЁЃ
(3)ЙЄвЕЩЯГЃгУАБЫЎЮќЪеКЌЬМШМСЯШМЩежаВњЩњЕФЮТЪвЦјЬхCO2ЃЌЕУЕНNH4HCO3ШмвКЃЌдђЗДгІNH4++HCO3Ѓ+H2ONH3ЁЄH2O+H2CO3ЕФЦНКтГЃЪ§K=_________ЁЃ(вбжЊГЃЮТЯТNH3ЁЄH2OЕФЕчРыЦНКтГЃЪ§Kb=2ЁС10Ѓ5ЃЌH2CO3ЕФЕчРыЦНКтГЃЪ§Ka1=4ЁС10Ѓ7ЃЌKa2=4ЁС10Ѓ11 )ЁЃ