题目内容
20.下列关于化学用语的使用正确的是( )| A. | 乙烯的结构式:CH2═CH2 | B. | Na2O的电子式: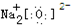 | ||
| C. | K+的电子排布式:1S22S22P63S23P6 | D. | 硝酸钾的分子式:KNO3 |
分析 A.结构式中需要用短线表示出所有的共用电子对;
B.钠离子不能合并,应该写在氧离子的两边;
C.钾离子的核外电子总数为18,结合构造原理形成其电子排布式;
D.硝酸钾为离子化合物,不存在分子式.
解答 解:A.CH2═CH2为结构简式,乙烯正确的结构式为: ,故A错误;
,故A错误;
B.氧化钠为离子化合物,钠离子直接用离子符号表示,阳离子需要标出最外层电子及所带的电荷,氧化钠的电子式为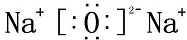 ,故B错误;
,故B错误;
C.K+的核外电子总数为18,其电子排布式为:1S22S22P63S23P6,故C正确;
D.硝酸钾为离子化合物,不存在分子式,KNO3为硝酸钾的化学式,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及电子式、结构式、电子排布式、化学式与分子式等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生的分析能力及规范答题能力.

练习册系列答案
相关题目
10.T℃时,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),发生反应:2SO2(g)+O2(g)?2SO3(g),5min时甲达到平衡.其起始量及SO2的平衡转化率如下表所示.下列叙述不正确的是( )
| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,甲、丙中气体密度分别为ρ1、ρ2,则ρ2>2ρ1 | |
| D. | 平衡时,SO2的转化率:α1<80%<α2 |
8.下列化学用语书写正确的是( )
| A. | NH4Cl的电子式: | |
| B. | 氮气的结构式::N≡N: | |
| C. | 氯化氢分子的形成过程可用电子式表示式: | |
| D. | 重水的化学式为 21H2O(或D2O) |
5.下列对有机反应类型的认识中错误的是( )
| A. |  +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$  +H2O;取代反应 +H2O;取代反应 | |
| B. | CH2═CH2+Br2→CH2Br-CH2Br;加成反应 | |
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;取代反应 | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化反应也属于取代反应 |
9.下列说法正确的是( )
| A. | 石油的催化重整和煤的干馏均可以得到芳香烃,说明石油和煤中含有芳香烃 | |
| B. | 石油裂解的目的主要是为了得到更多的汽油 | |
| C. | 石油分馏得到的产物可用来萃取溴水中的溴 | |
| D. | 石油裂化主要得到的是乙烯、丙烯等气态烃 |
10.用Pt做电极电解100moLCuSO4溶液,电解一段时间后两极均收集到标准状况下的气体2.24L,则下列有关说法错误的是( )
| A. | 原CuSO4溶液的浓度为1mol/L | |
| B. | 若要使电解后的溶液恢复至电解前的CuSO4溶液,则需加入9.8gCu(OH)2固体 | |
| C. | 电解过程中转移电子数为0.4NA个 | |
| D. | 假设电解过程中忽略溶液体积变化,则电解后所得溶液中C(H+)=0.1mol/L |

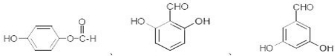 .
. 也可与化合物Ⅲ发生类
也可与化合物Ⅲ发生类 .
.