题目内容
8.下列化学用语书写正确的是( )| A. | NH4Cl的电子式: | |
| B. | 氮气的结构式::N≡N: | |
| C. | 氯化氢分子的形成过程可用电子式表示式: | |
| D. | 重水的化学式为 21H2O(或D2O) |
分析 A.氯离子为阴离子,电子式中需要标出氯离子的最外层8个电子;
B.结构式中不需要标出未成键电子对;
C.氯化氢为共价化合物,分子中不存在阴阳离子;
D.重水分子中的氢元素符号为D,其分子式为 21H2O(或D2O).
解答 解:A.氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为 ,故A错误;
,故A错误;
B.氮气分子中含有1个氮氮三键,其正确的结构式为:N≡N,故B错误;
C.氯化氢属于共价化合物,分子中不存在阴阳离子,用电子式表示氯化氢的形成过程为: ,故C错误;
,故C错误;
D.重水分子中含有的氢元素为D,则其化学式为:21H2O(或D2O),故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式结构式、化学式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案
相关题目
18.可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是( )
①一个N-N断裂的同时,有3个H-H键断裂
②一个N-N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均式量不再改变
④保持其它条件不变时,体系压强不再改变
⑤各物质的质量分数都不再改变
⑥恒温恒容时,密度保持不变
⑦正反应速率v(H2)=0.6mol/L•min,逆反应速率v(NH3)=0.4mol/L•min.
①一个N-N断裂的同时,有3个H-H键断裂
②一个N-N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均式量不再改变
④保持其它条件不变时,体系压强不再改变
⑤各物质的质量分数都不再改变
⑥恒温恒容时,密度保持不变
⑦正反应速率v(H2)=0.6mol/L•min,逆反应速率v(NH3)=0.4mol/L•min.
| A. | 全部 | B. | 只有①③④⑤ | C. | ②③④⑤⑦ | D. | 只有①③⑤⑥⑦ |
19.在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
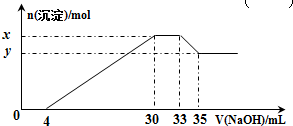

| A. | x与y的差值为0.1 mol | B. | 原溶液中c(Cl-)=0.75 mol•L-1 | ||
| C. | 原溶液的pH=1 | D. | 原溶液中n(Mg2+):n(Al3+)=5:2 |
16.下列材料中不含有SiO2的是( )
| A. | 普通玻璃 | B. | 氮化硅陶瓷 | C. | 光导纤维 | D. | 钢化玻璃 |
13.某烷烃主链上有4个碳原子的同分异构体有2种,含有相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 7种 |
20.下列关于化学用语的使用正确的是( )
| A. | 乙烯的结构式:CH2═CH2 | B. | Na2O的电子式: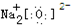 | ||
| C. | K+的电子排布式:1S22S22P63S23P6 | D. | 硝酸钾的分子式:KNO3 |
18.有机物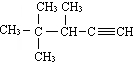 的系统名称为( )
的系统名称为( )
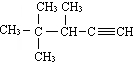 的系统名称为( )
的系统名称为( )| A. | 2,2,3一三甲基一1-戊炔 | B. | 2,2,3一三甲基一4一戊炔 | ||
| C. | 3,4,4一三甲基戊炔 | D. | 3,4,4一三甲基一l一戊炔 |

 .
.