题目内容
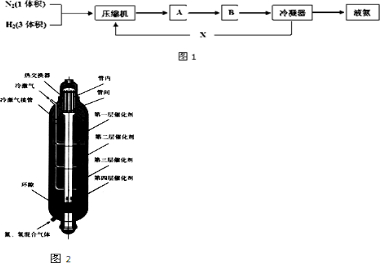
合成氨工业的主要反应为:N2(g)+3H2(g)?2NH3(g)△H<O,如图1是合成氨的简要流程示意图:
(1)沿X路线进入压缩机的物质是 .
(2)氮、氢混合气体送入合成塔前要通过压缩机压缩的原因是 ;
(3)如图为氨合成塔,为什么原料气从塔底流经外筒环隙进入,气体在反应前后都要通过热交换器?
.

(1)沿X路线进入压缩机的物质是
(2)氮、氢混合气体送入合成塔前要通过压缩机压缩的原因是
(3)如图为氨合成塔,为什么原料气从塔底流经外筒环隙进入,气体在反应前后都要通过热交换器?
考点:工业合成氨
专题:氮族元素
分析:(1)根据合成氨反应为可逆反应来回答;
(2)根据增大压强和减少生成物对反应速率或是平衡移动的影响知识来回答;
(3)合成氨气的适宜温度选择在500℃左右,使催化剂都能起到最大的催化作用是最终目的.
(2)根据增大压强和减少生成物对反应速率或是平衡移动的影响知识来回答;
(3)合成氨气的适宜温度选择在500℃左右,使催化剂都能起到最大的催化作用是最终目的.
解答:
解:(1)工业合成氨的流程中,原理是氮气与氢气反应生成氨气,此反应为可逆反应,故氮气与氢气应循环利用,故答案为:N2和H2;
(2)氮、氢混合气体送入合成塔前要通过压缩机压缩,来增大压强,这样可以加快化学反应速率,还可以让化学平衡朝生成NH3的方向进行,故答案为:增大压强,加快反应速率,使平衡朝生成NH3的方向进行;
(3)冷的原料气和反应气混合,可以进行热交换,保证反映的温度,让催化剂的催化活性最大,故答案为:进行热交换,预热原料气,加快反应速率;充分利用反应放出的热量,节约能源.
(2)氮、氢混合气体送入合成塔前要通过压缩机压缩,来增大压强,这样可以加快化学反应速率,还可以让化学平衡朝生成NH3的方向进行,故答案为:增大压强,加快反应速率,使平衡朝生成NH3的方向进行;
(3)冷的原料气和反应气混合,可以进行热交换,保证反映的温度,让催化剂的催化活性最大,故答案为:进行热交换,预热原料气,加快反应速率;充分利用反应放出的热量,节约能源.
点评:本题主要考查的是合成氨工业,应该熟悉合成氨的设备、原理,掌握平衡移动的原理,难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A、标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为
| ||
| B、1 mol甲基(-CH3)所含的电子总数为10NA | ||
| C、7 g CnH2n中含有的氢原子数目为NA | ||
| D、1mol金刚石晶体中,平均含有碳碳单键键数为4 NA |
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是( )
| A、NaOH |
| B、NH3?H2O |
| C、AgNO3 |
| D、BaCl2 |
下列关于有机物的说法正确的是( )
| A、乙烯和聚乙烯都能发生加成反应 |
| B、淀粉和纤维素的分子式相同,互为同分异构体 |
| C、粮食酿酒的过程涉及到了水解反应、氧化还原反应等复杂变化 |
| D、向蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4 溶液,蛋白质均发生变性 |
 已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基
已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A.B的基