题目内容
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A、标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为
| ||
| B、1 mol甲基(-CH3)所含的电子总数为10NA | ||
| C、7 g CnH2n中含有的氢原子数目为NA | ||
| D、1mol金刚石晶体中,平均含有碳碳单键键数为4 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标况下,庚烷是液态;
B、根据甲基呈电中性,1mol甲基含9mol电子来分析;
C、根据CnH2n的最简式为CH2来计算;
D、金刚石中,平均每个碳原子含有2个共价键;
B、根据甲基呈电中性,1mol甲基含9mol电子来分析;
C、根据CnH2n的最简式为CH2来计算;
D、金刚石中,平均每个碳原子含有2个共价键;
解答:
解:A、标况下,庚烷是液态,故1L庚烷的物质的量不是
mol,故所生成的气态产物的分子数为
NA,故A错误;
B、甲基呈电中性,1mol甲基含9mol电子,故B错误;
C、CnH2n的最简式为CH2,故7gCnH2n中含有的CH2的物质的量n=
=
=0.5mol,含有的氢原子的物质的量为1mol,数目为NA,故C正确;
D、金刚石中,平均每个碳原子含有2个共价键,所以1mol金刚石晶体中含碳碳键数为2NA,故D错误;
故选C.
| 1 |
| 22.4 |
| 7 |
| 22.4 |
B、甲基呈电中性,1mol甲基含9mol电子,故B错误;
C、CnH2n的最简式为CH2,故7gCnH2n中含有的CH2的物质的量n=
| m |
| M |
| 7g |
| 14g/mol |
D、金刚石中,平均每个碳原子含有2个共价键,所以1mol金刚石晶体中含碳碳键数为2NA,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的数值,下列说法中,正确的是( )
| A、标准状况下,22.4L Cl2完全反应时,转移电子数一定为2NA |
| B、常温下,l LpH=l的H2SO4溶液中含有的H+的数目为0.2NA |
| C、标准状况下,2.24 L NH3中含有共价键的数目为NA |
| D、常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 |
如图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O下列说法正确的是( )
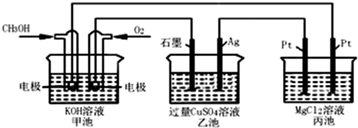

| A、甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B、甲池通入CH3OH的电极反应为CH3OH-6e?+2H2O═CO32?+8H+ |
| C、反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 |
| D、甲池中消耗224 mL(标准状况下)O2,此时乙池中银电极上产生1.28g固体 |
分子式C3H6Cl2的氯代烷分子中的一个氢原子被氯原子取代后,可得到两种同分异构体,则C3H6Cl2的名称是( )
| A、1,3-二氯丙烷 |
| B、1,1-二氯丙烷 |
| C、1,2-二氯丙烷 |
| D、2,2-二氯丙烷 |
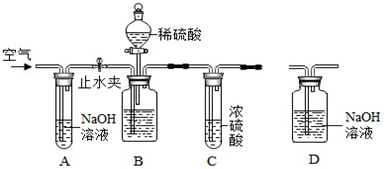
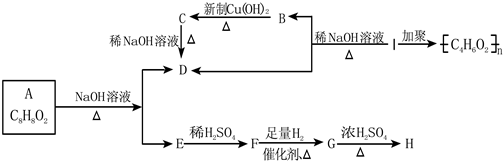 其中F能与FeCl3溶液显紫色,I为一种不饱和酯.
其中F能与FeCl3溶液显紫色,I为一种不饱和酯. 实验室制取乙烯:C2H5OH
实验室制取乙烯:C2H5OH