题目内容
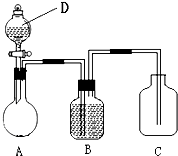 为确认C6H5OH、H2CO3、CH3COOH的酸性强弱,某同学设计了如图所示装置,一次实验即可达到目的(不必选用其他酸性物质).请据此实验回答下列问题:
为确认C6H5OH、H2CO3、CH3COOH的酸性强弱,某同学设计了如图所示装置,一次实验即可达到目的(不必选用其他酸性物质).请据此实验回答下列问题:(1)仪器D的名称是
(2)在烧瓶中装某可溶性正盐溶液,则A中反应的离子方程式是
(3)装置B中所盛的试剂是
(4)装置C中所盛的试剂是
(5)根据该实验可以得出C6H5OH、H2CO3、CH3COOH这三种物质的酸性强弱顺序为
考点:比较弱酸的相对强弱的实验
专题:实验探究和数据处理题
分析:根据强酸制取弱酸知中,强酸能和弱酸盐反应生成弱酸(酸相对强弱),弱酸能制取更弱的酸,要想验证C6H5OH、H2CO3、CH3COOH的酸性强弱,用CH3COOH和碳酸盐反应制取二氧化碳,用二氧化碳和苯酚的可溶性盐制取苯酚,注意常温下,苯酚不易溶于水,根据实验现象确定酸的相对强弱.
解答:
解:(1)D装置为分液漏斗,应盛放CH3COOH以与碳酸盐反应生成二氧化碳,证明CH3COOH酸性强于碳酸酸性,故答案为:分液漏斗;CH3COOH;
(2)用CH3COOH和可溶性碳酸盐反应制取二氧化碳,锥形瓶装有适量易溶于水的正盐固体,所以反应发生的离子反应方程式为CO32-+2CH3COOH=CO2↑+H2O+CH3COO-,
故答案为:CO32-+2CH3COOH=CO2↑+H2O+CH3COO-;
(3)醋酸有挥发性,导致二氧化碳气体中含有醋酸,会对实验造成干扰,所以B装置要盛放能除去醋酸,且不引起二氧化碳产生新的杂质、不能和二氧化碳反应的药品,一般常用碳酸氢钠溶液,该试剂的作用是除去二氧化碳中的醋酸杂质,故答案为:饱和碳酸氢钠溶液;除去CO2中混有的醋酸杂质;
(3)二氧化碳和苯酚钠溶液反应生成不溶性的苯酚,所以C选用苯酚钠溶液,反应方程式为C6H5ONa+H2O+CO2→C6H5OH+NaHCO3,
故答案为:苯酚钠溶液;C6H5ONa+H2O+CO2→C6H5OH+NaHCO3;
(4)由于CH3COOH能与碳酸盐反应生成二氧化碳,二氧化碳与苯酚钠反应生成C6H5OH,所以酸性强弱顺序为CH3COOH>H2CO3>C6H5OH,故答案为:CH3COOH>H2CO3>C6H5OH.
(2)用CH3COOH和可溶性碳酸盐反应制取二氧化碳,锥形瓶装有适量易溶于水的正盐固体,所以反应发生的离子反应方程式为CO32-+2CH3COOH=CO2↑+H2O+CH3COO-,
故答案为:CO32-+2CH3COOH=CO2↑+H2O+CH3COO-;
(3)醋酸有挥发性,导致二氧化碳气体中含有醋酸,会对实验造成干扰,所以B装置要盛放能除去醋酸,且不引起二氧化碳产生新的杂质、不能和二氧化碳反应的药品,一般常用碳酸氢钠溶液,该试剂的作用是除去二氧化碳中的醋酸杂质,故答案为:饱和碳酸氢钠溶液;除去CO2中混有的醋酸杂质;
(3)二氧化碳和苯酚钠溶液反应生成不溶性的苯酚,所以C选用苯酚钠溶液,反应方程式为C6H5ONa+H2O+CO2→C6H5OH+NaHCO3,
故答案为:苯酚钠溶液;C6H5ONa+H2O+CO2→C6H5OH+NaHCO3;
(4)由于CH3COOH能与碳酸盐反应生成二氧化碳,二氧化碳与苯酚钠反应生成C6H5OH,所以酸性强弱顺序为CH3COOH>H2CO3>C6H5OH,故答案为:CH3COOH>H2CO3>C6H5OH.
点评:本题考查了比较弱酸相对强弱的探究实验,难度不大,注意苯酚钠和二氧化碳、水反应生成碳酸氢钠不是碳酸钠.

练习册系列答案
相关题目
25℃,取浓度相等的NaOH和HCl溶液,以3:2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为( )
| A、0.01mol/L |
| B、0.017moL/L |
| C、0.05mol/L |
| D、0.50moL/L |
下列离子方程式正确的是( )
| A、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、Ag2S沉淀溶解平衡表达式:Ag2S?2Ag++S2- |
| C、氢硫酸与硫酸铜反应:S2-+Cu2+=CuS↓ |
| D、NaHCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
一种气态烷烃和一种气态烯烃的混合物共14.3g,同温同压下,该混合气体密度为氢气密度的11倍,将混合气通过足量溴水,溴水增重6.3g.则混合气中的烃分别是( )
| A、甲烷和乙烯 |
| B、甲烷和丙烯 |
| C、甲烷和丁烯 |
| D、乙烷和丙烯 |
下列说法正确的是( )
| A、0.01mol/L的Na2HPO4溶液中存在如下的平衡;HPO42-?H++PO43-,加水稀释,使溶液中的HPO42-、H+、PO43-的浓度均减小 |
| B、饱和NH4Cl中:c(H+)+c(Cl-)=c(NH4+)+2c(NH3?H2O)+c(OH-) |
| C、常温下,0.1mol/L的HA和BOH两种溶液,其pH值分别为3和12,将两溶液等体积混合后,所得溶液的pH≤7 |
| D、在NH4HSO3与NH4Cl混合溶液中:c(NH4+)=c(SO32-)+c(HSO3-)+c(H2SO3)+c(Cl-) |
如图所示,下列实验操作与方法正确的是( )
A、 |
B、 |
C、 |
D、 |
