题目内容
3.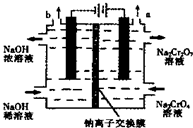 某工厂采用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,其装置如图所示.下列说法正确的是( )
某工厂采用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,其装置如图所示.下列说法正确的是( )| A. | 阳极区的pH会不断下降 | |
| B. | 溶液中Na+从阴极移向阳极 | |
| C. | 该电解池的两电极材料只能用石墨不能用铁 | |
| D. | 阳极区发生的反应是:2H2O-4e-═O2↑+4H+,2CrO42-+2H+═Cr2O72-+H2O |
分析 用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,则阳极上失去电子发生氧化反应,阴极上氢离子放电生成氢气,阳离子向阴极移动,若选Fe作电解,阳极上Fe失去电子生成亚铁离子与Na2CrO4发生氧化还原反应,不能实现Na2CrO4到 Na2Cr2O7的转化,以此来解答.
解答 解:A.阳极区发生2H2O-4e-═O2↑+4H+、2CrO42-+2H+═Cr2O72-+H2O,pH变化不大,故A错误;
B.溶液中Na+从阳极移向阴极,故B错误;
C.选Fe作电解,阳极上Fe失去电子生成亚铁离子与Na2CrO4发生氧化还原反应,不能实现Na2CrO4到 Na2Cr2O7的转化,故C错误;
D.阳极区发生的反应是:2H2O-4e-═O2↑+4H+,2CrO42-+2H+═Cr2O72-+H2O,从而实现Na2CrO4到 Na2Cr2O7的转化,故D正确;
故选D.
点评 本题考查电解原理的应用,为高频考点,把握发生的电极反应、工作原理为解答的关键,侧重分析与应用能力的考查,注意该电解实验的目的,题目难度不大.

练习册系列答案
相关题目
13.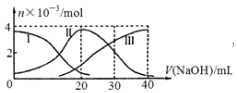 手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
 手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )| A. | H2A在水中的电离方程式是:H2A═2H++A2- | |
| B. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 | |
| C. | 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | 当V(NaOH)=30mL时,则有:c(H+)+c(Na+)═c(A2-)+c(OH-)+c(HA-) |
14. 与氢气加成产物的名称是( )
与氢气加成产物的名称是( )
 与氢气加成产物的名称是( )
与氢气加成产物的名称是( )| A. | 4-甲基己烷 | B. | 2-乙基戊烷 | C. | 1,3-二甲基戊烷 | D. | 3-甲基己烷 |
11.下列实验操作后溶液的颜色无明显变化的是( )
| A. | 硫酸铁溶液中滴加硫氰化钾溶液 | B. | 氯化铝中滴加石蕊指示剂 | ||
| C. | 偏铝酸钠溶液中滴加酚酞指示剂 | D. | 氯化亚铁溶液中滴加硫氰化钾溶液 |
18.在复杂体系中,确定化学反应先后顺序有利于解决问题.已知氧化性Fe3+>Cu2+>Fe2+.若在氯化铁溶液蚀刻铜印刷电路板后所得的溶液里加入过量锌片.下列说法正确的是( )
| A. | Fe3+首先反应,转化为Fe | B. | 反应开始时c(Fe2+)增大,然后又减小 | ||
| C. | Fe2+首先反应,转化为Fe | D. | 存在反应Fe+Cu2+→Fe2++Cu |
12.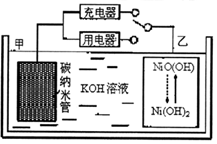 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A. | 电池总反应为H2+2NiOOH$?_{放电}^{充电}$2Ni(OH)2 | |
| B. | 放电时,甲电极为负极,OH-移向乙电极 | |
| C. | 放电时,乙电极反应为:NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| D. | 充电时,电池的碳电极与直流电源的正极相连 |
13.下列说法正确的是( )
| A. | 按系统命名法,有机物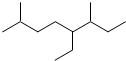 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | 麻黄碱(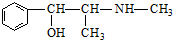 )的催化氧化产物能发生银镜反应 )的催化氧化产物能发生银镜反应 | |
| D. | 某分子式为C10H20O2的酯可发生如图所示的转化过程,则符合条件的酯的结构有4种 |