题目内容
实验室用浓硫酸和乙醇反应制备乙烯,反应为:CH3─CH2OH| 浓硫酸 |
| 170℃ |
若温度过高或加热时间过长,制得的乙烯往往混有少量CO2、SO2、H2O(气体).请回答下列问题:
I、怎样除去乙烯中的CO2和SO2?
II、写出乙烯通入溴水中反应的化学方程式
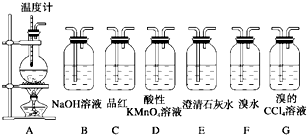
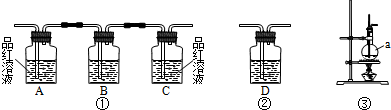
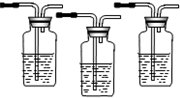
III、试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g),
(1)按气流的方向,各装置的连接顺序是:
 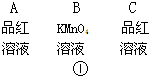 |
② |
③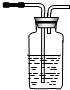 |
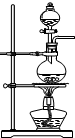 ④ ④ |
(3)装置②中所加的试剂名称是
(4)装置③中所盛溶液的名称是
分析:I、根据CO2和SO2都能与碱反应,乙烯与碱不反应来解答;
II、乙烯与单质溴发生加成反应生成1,2-二溴乙烷;
III、(1)(2)(3)(4)检验二氧化硫可用品红溶液,检验二氧化碳可以用澄清石灰水,检验水用无水硫酸铜,三者都有时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,二氧化碳的检验应放在排除SO2的干扰后进行,所以应先通过品红溶液褪色检验SO2的存在,再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用澄清石灰水实验检验二氧化碳;
II、乙烯与单质溴发生加成反应生成1,2-二溴乙烷;
III、(1)(2)(3)(4)检验二氧化硫可用品红溶液,检验二氧化碳可以用澄清石灰水,检验水用无水硫酸铜,三者都有时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,二氧化碳的检验应放在排除SO2的干扰后进行,所以应先通过品红溶液褪色检验SO2的存在,再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用澄清石灰水实验检验二氧化碳;
解答:解:I、CO2和SO2都能与碱反应,乙烯与碱不反应,所以通过氢氧化钠溶液可除去乙烯中的CO2和SO2;
故答案为:通过氢氧化钠溶液;
II、乙烯与单质溴发生加成反应生成1,2-二溴乙烷,方程式为:CH2=CH2+Br2→CH2Br-CH2Br,该反应为加成反应;
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;加成反应;
III、(1)检验二氧化硫可用品红溶液,检验二氧化碳可以用澄清石灰水,检验水用无水硫酸铜,三者都有时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,二氧化碳的检验应放在排除SO2的干扰后进行,所以应先通过品红溶液褪色检验SO2的存在,再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用澄清石灰水实验检验二氧化碳;
故答案为:④②①③;
(2)检验二氧化硫可用品红溶液,二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,二氧化碳的检验应放在排除SO2的干扰后进行,所以应先通过品红溶液褪色检验SO2的存在,再通过酸性高锰酸钾溶液除去SO2,接着通过品红溶液不褪色确认SO2已除干净;
故答案为:检验是否有SO2;除去或吸收SO2;检验SO2是否除尽;
(3)检验水用无水硫酸铜,白色固体变为蓝色说明含有水蒸气;验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气,应最先用用无水硫酸铜检验水;
故答案为:无水硫酸铜;水蒸气;
(4)检验二氧化碳可以用澄清石灰水溶液,在排除二氧化硫的干扰后,澄清石灰水变浑浊,说明含有二氧化碳,
故答案为:澄清的石灰水;CO2.
故答案为:通过氢氧化钠溶液;
II、乙烯与单质溴发生加成反应生成1,2-二溴乙烷,方程式为:CH2=CH2+Br2→CH2Br-CH2Br,该反应为加成反应;
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;加成反应;
III、(1)检验二氧化硫可用品红溶液,检验二氧化碳可以用澄清石灰水,检验水用无水硫酸铜,三者都有时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,二氧化碳的检验应放在排除SO2的干扰后进行,所以应先通过品红溶液褪色检验SO2的存在,再通过酸性高锰酸钾溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用澄清石灰水实验检验二氧化碳;
故答案为:④②①③;
(2)检验二氧化硫可用品红溶液,二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,二氧化碳的检验应放在排除SO2的干扰后进行,所以应先通过品红溶液褪色检验SO2的存在,再通过酸性高锰酸钾溶液除去SO2,接着通过品红溶液不褪色确认SO2已除干净;
故答案为:检验是否有SO2;除去或吸收SO2;检验SO2是否除尽;
(3)检验水用无水硫酸铜,白色固体变为蓝色说明含有水蒸气;验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气,应最先用用无水硫酸铜检验水;
故答案为:无水硫酸铜;水蒸气;
(4)检验二氧化碳可以用澄清石灰水溶液,在排除二氧化硫的干扰后,澄清石灰水变浑浊,说明含有二氧化碳,
故答案为:澄清的石灰水;CO2.
点评:本题考查乙烯的化学性质、制备以及常见气体的检验,题目难度不大,注意实验原理及检验的先后顺序.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
实验室可用乙醇来制取乙烯,工业上可用乙醇来制取乙醛.实验室用浓硫酸和乙醇制乙烯时,常会看到烧瓶中液体变黑,并在制得的乙烯中混有CO2、SO2等杂质.请从图1中选用所需要的仪器(可重复选用)组成一套能进行上述反应,并检出所得混合气体中含有乙烯、SO2、CO2、H2O(g)的装置(连接用的玻璃管、橡胶管等略去).供选用的试剂:浓硫酸、无水乙醇、无水硫酸铜、酸性KMnO4溶液、FeCl3溶液、溴水、品红溶液、澄清石灰水、NaOH溶液、浓盐酸.按仪器连接顺序从上到下将下表补充完整.

Ⅱ.用图2装置进行乙醇的催化氧化实验并制取乙醛(图中铁架台等装置已略去,粗黑线表示乳胶管).请填写下列空白:
(1)甲装置常常浸在70~80℃的水浴中,目的是 ;
(2)乙中发生的反应的化学方程式为 ;
(3)若鼓气速度过快则会 ;
(4)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接 、 接丙;若产物不用水吸收而是直接冷却,应将试管丁浸在 中,检验乙醇催化氧化产物的试剂是 ,其化学方程式为 .

| 序号 | 选用的仪器(填字母) | 加入的试剂 | 作用 |
| ① | B | 浓硫酸、无水乙醇 | 反应器 |
| ② | 无水硫酸铜 | 检出水蒸气 | |
| ③ | C | 品红溶液 | |
| ④ | C | 吸收SO2 | |
| ⑤ | C | 品红溶液 | |
| ⑥ | C | 检出乙烯 | |
| ⑦ | C | 澄清石灰水 | 检出CO2 |
(1)甲装置常常浸在70~80℃的水浴中,目的是
(2)乙中发生的反应的化学方程式为
(3)若鼓气速度过快则会
(4)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接