题目内容
16.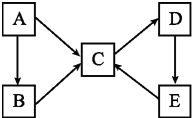 A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系:
A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系:(1)若A为单质,C、D的相对分子质量相差16.0.05 mol•L-1 E溶液中只有3种离子,且在25℃时,溶液中的$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012.
①若B为气态氢化物,写出E→C的一个化学方程式Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O或C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
②在A→C的反应中,每转移1 mol e-就会放热143.5 kJ,写出该反应的热化学方程式S(g)+O2(g)═SO2(g)△H=-574.0 kJ/mol.
(2)若A为单质,B、C均属于盐类,D是一种白色沉淀.
①若B的水溶液呈酸性,C的水溶液呈碱性,C溶液呈碱性的原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式表示).
②若B溶液呈黄色,与硫氰化钾溶液混合后显红色,E是一种不溶性碱.则:
(Ⅰ)B→C的离子方程式为2Fe3++Fe═3Fe2+.
(Ⅱ)D→E的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(Ⅲ)选用一种试剂R与E反应实现E→C的转化,则R为HI;该反应的离子方程式为2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O.
(3)若A~E均为化合物,且均含有元素Y.A是淡黄色固体,B、C两溶液在等物质的量浓度时,C溶液的pH较小.电解D的水溶液是最重要的工业生产之一,D→E→C也是工业制备C的普遍方法.Y的单质与钾的合金可在核反应堆中用作热交换液.5.05 g Y钾合金溶于200 mL水生成0.075 mol氢气,计算并确定该Y钾合金的化学式是NaK2.
分析 (1)A为单质,C、D的相对分子质量相差16,0.05mol/L E溶液中只有3种离子,且且溶液中的溶液中的$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012,则溶液中的c(H+)=0.1mol/L,E为二元强酸,若B为气态氢化物,则A为S,C为SO2,D为SO3,B为H2S,E为硫酸;
(2)若A为单质,B、C均属于盐类,D是一种白色沉淀.
①若B的水溶液呈酸性,C的水溶液呈碱性,则Al,B为AlCl3,C为NaAlO2,D为Al(OH)3,E为Al2O3;
②若B溶液呈黄色,与硫氰化钾溶液混合后显红色,可说明B中含有Fe3+,A应为Fe,C中含有Fe2+,E是一种不溶性碱,由转化关系可知D为Fe(OH)2,E为Fe(OH)3,用HI与氢氧化铁反应可以实现E、C转化;
(3)A~E均为化合物,且均含有元素Y,A是淡黄色固体,则A为Na2O2,Y为Na.B、C两溶液在等物质的量浓度时,C溶液的pH较小,B为Na2CO3,C为NaHCO3,电解D的水溶液是最重要的工业生产之一,D应为NaCl,D→E→C也是工业制备C的普遍方法,为侯氏制碱法,E为NaOH.
解答 解:(1)A为单质,C、D的相对分子质量相差16,0.05mol/L E溶液中只有3种离子,且且溶液中的溶液中的$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012,则溶液中的c(H+)=0.1mol/L,E为二元强酸,若B为气态氢化物,则A为S,C为SO2,D为SO3,B为H2S,E为硫酸.
①E→C的化学方程式为Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O或C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O或C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
②A→C的反应为S(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$SO2(g),每转移1mol e-就会放热143.5kJ,则转移4mol电子吸收143.5kJ×4=574.0kJ热量,则反应的热化学方程式为S(g)+O2(g)═SO2(g)△H=-574.0 kJ/mol,
故答案为:S(g)+O2(g)═SO2(g)△H=-574.0 kJ/mol;
(2)若A为单质,B、C均属于盐类,D是一种白色沉淀.
①若B的水溶液呈酸性,C的水溶液呈碱性,则Al,B为AlCl3,C为NaAlO2,D为Al(OH)3,E为Al2O3,B溶液呈酸性的原因是铝离子水解使溶液呈酸性,离子方程式为Al3++3H2O?Al(OH)3+3H+,
故答案为:Al3++3H2O?Al(OH)3+3H+;
②若B溶液呈黄色,与硫氰化钾溶液混合后显红色,可说明B中含有Fe3+,A应为Fe,C中含有Fe2+,E是一种不溶性碱,由转化关系可知D为Fe(OH)2,E为Fe(OH)3,用HI与氢氧化铁反应可以实现E、C转化.
(I)B→C的离子方程式为2Fe3++Fe═3Fe2+,故答案为:2Fe3++Fe═3Fe2+;
(Ⅱ)D→E的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(Ⅲ)用HI与Fe(OH)3反应,反应的离子方程式为2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O,
故答案为:HI;2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O;
(3)A~E均为化合物,且均含有元素Y,A是淡黄色固体,则A为Na2O2,Y为Na.B、C两溶液在等物质的量浓度时,C溶液的pH较小,B为Na2CO3,C为NaHCO3,电解D的水溶液是最重要的工业生产之一,D应为NaCl,D→E→C也是工业制备C的普遍方法,为侯氏制碱法,E为NaOH.5.05 g 钠钾合金溶于200 mL水生成0.075 mol氢气,设Na、K物质的量分别为xmol、ymol,则:$\left\{\begin{array}{l}{23x+39y=5.05}\\{x+y=0.075×2}\end{array}\right.$,解得x=0.05,y=0.1,故钠钾合金的化学式是NaK2,
故答案为:NaK2.
点评 本题考查无机物的推断,注意利用信息及转化关系图推断各物质,熟练掌握元素化合物性质,题目难度中等.

| A. | 氧化性:Na+>H+>Cu2+ | |
| B. | 还原性:Cl->S2->O2- | |
| C. | 等质量时的耗氧量:C2H6>CH4>C6H6 | |
| D. | 与金属钠反应的剧烈程度:C2H5OH<H2O |
| A. | 8种 | B. | 10种 | C. | 11种 | D. | 12种 |
 臭氧是一种强氧化剂,常用于消毒、灭菌等.
臭氧是一种强氧化剂,常用于消毒、灭菌等.(1)已知O3与KI溶液反应的生成物中有两种单质是I2和O2.
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示.
已知:O3的起始浓度为0.0216mol/L.
pH t/min T/℃ | 3,.0 | 4,.0 | 5,.0 | 6,.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
②在30°C、pH=4.0条件下,O3的分解速率为1.00×10-4 mol/(L•min).
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为bac.(填字母代号)
a.40°C、pH=3.0 b.10°C、pH=4.0 c.30°C、pH=7.0
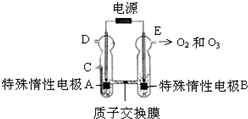
(3)O3可由臭氧发生器(原理如下图)电解稀硫酸制得.
①图中阴极为A(填“A”或“B”),其电极反应式为2H++2e-=H2↑.
②若C处通入O2,则A极的电极反应式为O2+4H++4e-=2H2O.
| A. | 甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 | |
| B. | 蔗糖、麦芽糖的分子式都是C12H22O11,它们互为同分异构体 | |
| C. | “地沟油”可通过水解制得肥皂 | |
| D. | 苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应 |
| A. | 在一定量的Ba(OH)2溶液中通入过量SO2气体SO2+OH-═HS${{O}_{3}}^{-}$ | |
| B. | 4 mol•L-1的NaAlO2溶液和7 mol•L-1的盐酸等体积混合4 Al${O}_{2}^{-}$+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 在碳酸氢钠溶液中加入等物质的量的氢氧化钙溶液Ca2++HC${O}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| D. | 用惰性电极电解氯化铝溶液2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- |
| A. | 氢有三种同素异形体,分别是氕、氘、氚 | |
| B. | 氢有三种同位素,它们的相对原子质量分别是1、2、3 | |
| C. | 氢元素可形成三种互为通分异构体的物质:H2、D2、T2 | |
| D. | 氢元素的三种同位素原子可用一个原子结构示意图表示 |
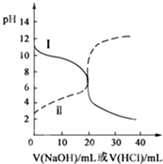 25℃时,取浓度均为0.1mol/L的醋酸溶液和氨水溶液各20mL,分别用0.1mol/LNaOH溶液、0.1mol/L盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol/L的醋酸溶液和氨水溶液各20mL,分别用0.1mol/LNaOH溶液、0.1mol/L盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | 曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 曲线Ⅰ:滴加溶液到20 mL时:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| C. | 曲线Ⅱ:滴加溶液在10 mL~20 mL之间时:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| D. | 曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
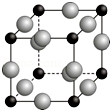 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):