题目内容
在MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O的反应中,用“双线桥法”表示氧化还原反应中电子转移情况;还原剂是
| ||
HCl
HCl
,氧化产物是Cl2
Cl2
,该反应的离子方程式为MnO2+4H++2Cl-(浓)
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-(浓)
Mn2++Cl2↑+2H2O
.
| ||
分析:在氧化还原反应中,化合价升高值=化合价降低值=转移电子数,化合价升高元素所在反应物是还原剂,对应氧化产物,根据反应方程式来书写离子方程式.
解答:解:在MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O的反应中,锰元素化合价降低,氯元素化合价升高,转移电子数为2mol,用“双线桥法”表示氧化还原反应中电子转移情况为: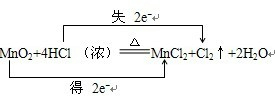 ,氯元素化合价升高,还原剂是HCl,氧化产物是Cl2,反应的实质是:MnO2+4H++2Cl-(浓)
,氯元素化合价升高,还原剂是HCl,氧化产物是Cl2,反应的实质是:MnO2+4H++2Cl-(浓)
Mn2++Cl2↑+2H2O.
故答案为:HCl;Cl2;MnO2+4H++2Cl-(浓)
Mn2++Cl2↑+2H2O.
| ||
 ,氯元素化合价升高,还原剂是HCl,氧化产物是Cl2,反应的实质是:MnO2+4H++2Cl-(浓)
,氯元素化合价升高,还原剂是HCl,氧化产物是Cl2,反应的实质是:MnO2+4H++2Cl-(浓)
| ||
故答案为:HCl;Cl2;MnO2+4H++2Cl-(浓)
| ||
点评:本题考查学生离子反应和氧化还原反应的概念,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
在MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O反应中,被氧化的HCl与参加反应的HCl物质的量关系是( )
| ||
| A、1:2 | B、1:1 |
| C、1:4 | D、1:3 |