题目内容
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和KCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,
则①Y电极上的电极反应式为
②该反应的总反应化学方程式是:
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是
(3)若用惰性电极电解500mL CuSO4溶液,溶液中 Cu2+完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极质量增加1.6g.
①要使电解后溶液恢复到电解前的状态,需加入一定量的
②溶液的pH=
考点:电解原理
专题:
分析:(1)①若X、Y都是惰性电极,a是饱和KCl溶液,Y电极上氯离子放电生成氯气,X电极上氢离子放电,同时该电极附近生成氢氧根离子;
②根据阴阳极反应写出总反应;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电;
(3)根据电池反应式电解出的物质判断并计算析出物质的质量;根据电池反应式中铜与氢离子的关系式计算氢离子的物质的量,从而确定溶液的PH值;
②根据阴阳极反应写出总反应;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电;
(3)根据电池反应式电解出的物质判断并计算析出物质的质量;根据电池反应式中铜与氢离子的关系式计算氢离子的物质的量,从而确定溶液的PH值;
解答:
解:(1)①若X、Y都是惰性电极,a是饱和KCl溶液,和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,所以此电极有黄绿色气体产生,故答案为:2Cl--2e-=Cl2↑,有黄绿色气体生成;
②阳极反应式:2Cl--2e-=Cl2↑,阴极反应式:2H++2e-=H2↑,而来自于KCl,H+来自于H2O,故总反应为:2KCl+2H2O
2KOH+Cl2↑+H2↑,故答案为:2KCl+2H2O
2KOH+Cl2↑+H2↑;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,即X电极是纯铜、Y电极是粗铜,阴极发生反应为:Cu2++2e-=Cu,故答案为:纯铜;Cu2++2e-=Cu;
(3)①根据电池反应式知,析出的物质是铜和氧气,要使电解后溶液恢复到电解前的状态,则需加入 CuO;
②2Cu2++2H2O
2Cu+O2↑+4H+
128g 4mol
1.6g 0.05mol
C(H + )=
=
=0.1mol/L,所以pH=1;
故答案为:CuO;1;
②阳极反应式:2Cl--2e-=Cl2↑,阴极反应式:2H++2e-=H2↑,而来自于KCl,H+来自于H2O,故总反应为:2KCl+2H2O
| ||
| ||
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,即X电极是纯铜、Y电极是粗铜,阴极发生反应为:Cu2++2e-=Cu,故答案为:纯铜;Cu2++2e-=Cu;
(3)①根据电池反应式知,析出的物质是铜和氧气,要使电解后溶液恢复到电解前的状态,则需加入 CuO;
②2Cu2++2H2O
| ||
128g 4mol
1.6g 0.05mol
C(H + )=
| n |
| V |
| 0.05mol |
| 0.5L |
故答案为:CuO;1;
点评:本题考查了电解池工作原理中阴阳极的判断、电极反应式的书写等知识点,本题中利用得失电子守恒、溶液中阴阳离子所带电荷守恒是解(3)题的关键.

练习册系列答案
相关题目
2014年6月5日为世界环境日,主题为“提高你的呼声而不是海平面”,提倡节能减排,以下措施中不能体现这一思想的是( )
| A、在电解铝工业中添加冰晶石 |
| B、大力发展火电,缓解用电紧张 |
| C、开发太阳能、风能、氢能等清洁能源 |
| D、研制出性能优良的催化剂,降低反应所需温度 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol OH一中含有9 NA个电子 |
| B、1 L 1 mol?L-1CH3COONa溶液中含有NA个CH3COO- |
| C、28g CO气体中含有NA个氧原子 |
| D、常温常压下11.2 L甲烷气体含有的分子数为0.5NA |
电解饱和食盐水的装置如右图,通电一段时间后,下列说法一定正确的是( )


| A、滴加适量盐酸,可以使电解质溶液复原 |
| B、在U形管两端分别滴加酚酞试液,右端变红 |
| C、可用中和滴定的方法测定生成的氢氧化钠溶液的物质的量浓度 |
| D、若得到22.4 LH2(标准状况下),理论上需要转移NA个电子(NA为阿伏加德罗常数的值) |
化学与生产、生活密切相关,下列叙述错误的是( )
| A、用热的纯碱溶液清除灶具上的油污 |
| B、用硫酸清洗锅炉中的水垢 |
| C、用明矾[KAl(SO4)2.12H2O]作净水剂,除去水中悬浮的杂质 |
| D、用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+ |
25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
A、 表示的粒子不会对水的电离平衡产生影响 表示的粒子不会对水的电离平衡产生影响 |
B、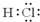 表示的物质加入水中,促进水的电离,c(H+)增大 表示的物质加入水中,促进水的电离,c(H+)增大 |
C、25℃时, 表示的微粒加入水中,促进水的电离,Kw不变 表示的微粒加入水中,促进水的电离,Kw不变 |
| D、水的电离程度只与温度有关,温度越高,电离程度越大 |
下列反应能用CO32-+2H+═CO2↑+H2O表示的是( )
| A、Na2CO3+H2SO4═Na2SO4+CO2↑+H2O |
| B、CaCO3+2HCl═CaCl2+CO2↑+H2O |
| C、KHCO3+HCl═KCl+CO2↑+H2O |
| D、BaCO3+2HNO3═Ba(NO3 )2+CO2↑+H2O |


