题目内容
4.质量分数为14%的KOH 溶液,蒸发掉63g水,质量分数恰好增大一倍,体积变为500mL,则浓缩后溶液的物质的量溶液为0.63mol/L.分析 根据蒸发前后溶质的质量不变,计算出原溶液的质量,根据m(溶质)=m(溶液)•ω计算溶质质量,根据n=$\frac{m}{M}$计算溶质KOH的物质的量,进而根据c=$\frac{n}{V}$计算溶液的物质的量浓度.
解答 解:蒸发掉63g水后质量分数恰好增大一倍,蒸发水后溶质质量分数为28%,
设14%氢氧化钾溶液的质量为m,蒸发前后溶质的质量不变,则:m×14%=(m-63g)×28%,解得:m=126g,
则28%的氢氧化钾溶液中含有氢氧化钾的物质的量为:$\frac{(126-63)g×28%}{56g/mol}$=0.315mol,
所得溶液的物质的量浓度为:c(KOH)=$\frac{0.315mol}{0.5L}$=0.63mol/L,
故答案为:0.63mol/L.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确溶质质量分数的概念及表达式为解答关键,注意掌握物质的量浓度的计算方法,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀HCl,完全反应后,离子数目几乎没有改变的是( )
| A. | Fe2+ | B. | Fe3+ | C. | Al3+ | D. | NH4+ |
6.二甲酸钾是一种白色晶体,商品名为弗米(Formil),是一种能替代抗生素的促生长剂,化学式为KH(HCOO)2,具有吸湿性,易溶于水.
二甲酸钾的生产工艺流程如下:
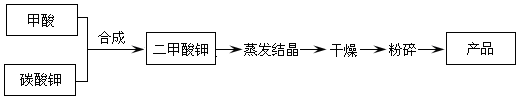
(1)以甲酸和碳酸钾为原料生产二甲酸钾,实验测得反应条件对产品回收率的影响如下:
表1 反应温度对产品回收率的影响
表2 反应物料比对产品回收率的影响
备注:表2中反应物料比为甲酸和无水碳酸钾的物质的量之比.
①写出甲酸和碳酸钾生产二甲酸钾的化学方程式:4HCOOH+K2CO3=2KH(HCOO)2+CO2↑+H2O.
②实际生产二甲酸钾时应选择的最佳反应条件是反应温度应控制在50℃∽60℃,反应物料比应选择4:1.由表1可知反应温度过高,反应回收率反而会降低,其原因可能是温度过高,甲酸易挥发.
(2)测定某弗米产品纯度的实验方法如下:
称取该弗米产品2.5g,将其全部溶解在水中,配制成250mL未知浓度的溶液,取出25.00mL于锥形瓶中,再滴加2~3滴指示剂,用0.10mol•L-1的NaOH溶液滴定至终点,消耗NaOH溶液的体积为18.50mL.
①加入的指示剂是酚酞(选填“甲基橙”、“石蕊”或“酚酞”),用NaOH溶液滴定至终点的现象是溶液由无色恰好变成浅红色且在半分钟内不褪色.
②上述弗米产品中二甲酸钾的质量分数为96.2%.
二甲酸钾的生产工艺流程如下:

(1)以甲酸和碳酸钾为原料生产二甲酸钾,实验测得反应条件对产品回收率的影响如下:
表1 反应温度对产品回收率的影响
| 反应温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 产品回收率(%) | 75.6 | 78.4 | 80.6 | 82.6 | 83.1 | 82.1 | 73.7 |
| 反应物料比 | 2:1 | 3:1 | 4:1 | 5:1 | 6:1 | 7:1 |
| 产品回收率(%) | 0 | 38.4 | 82. 6 | 83.6 | 84.5 | 84.8 |
①写出甲酸和碳酸钾生产二甲酸钾的化学方程式:4HCOOH+K2CO3=2KH(HCOO)2+CO2↑+H2O.
②实际生产二甲酸钾时应选择的最佳反应条件是反应温度应控制在50℃∽60℃,反应物料比应选择4:1.由表1可知反应温度过高,反应回收率反而会降低,其原因可能是温度过高,甲酸易挥发.
(2)测定某弗米产品纯度的实验方法如下:
称取该弗米产品2.5g,将其全部溶解在水中,配制成250mL未知浓度的溶液,取出25.00mL于锥形瓶中,再滴加2~3滴指示剂,用0.10mol•L-1的NaOH溶液滴定至终点,消耗NaOH溶液的体积为18.50mL.
①加入的指示剂是酚酞(选填“甲基橙”、“石蕊”或“酚酞”),用NaOH溶液滴定至终点的现象是溶液由无色恰好变成浅红色且在半分钟内不褪色.
②上述弗米产品中二甲酸钾的质量分数为96.2%.
12.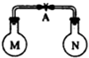 室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
 室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | H2 | NH3 | NO |
| 气体N | SO2 | Cl2 | HCl | O2 |
| A. | ②④①③ | B. | ①②③④ | C. | ④①②③ | D. | ①④③② |
19.下列反应离子方程式错误的是( )
| A. | 少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=2HClO+SO32- | |
| B. | 碳酸钙中滴入醋酸溶液:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ | |
| C. | 碳酸氢镁溶液中加入过量的澄清石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O | |
| D. | 硫酸亚铁溶液中加过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
14.在工农业生产和日常生活中有很多化学问题.下列说法正确的是( )
| A. | 明矾净水与液氯净水的原理相同 | |
| B. | 将草木灰和硫铵混合施用,肥效更高 | |
| C. | 冬季形成的大雾属于气溶胶 | |
| D. | 电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
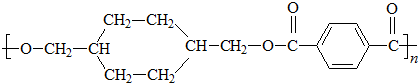
 、D
、D 、E
、E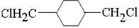 ;
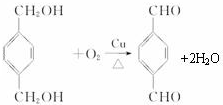
;
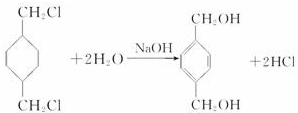 ;
; $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$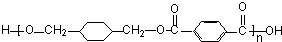 +(2n-1)H2O.
+(2n-1)H2O.