题目内容
下列反应的离子方程式正确的是( )
| A、氧化铜与稀硫酸反应:CuO+2H+=Cu2++H2O |
| B、石灰石溶于醋酸溶液:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、单质铁溶于稀硝酸溶液中:2Fe+6H+=2Fe3++3H2↑ |
| D、氢氧化钡与盐酸发生中和反应:Ba(OH)2+2H+=Ba2++2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、氧化铜为氧化物,在离子方程式中保留化学式;
B、醋酸为弱酸,离子方程式中需要保留分子式;
C、铁与稀硝酸反应生成是一氧化氮气体,不会生成氢气;
D、氢氧化钡为易溶物,离子方程式中写成离子形式.
B、醋酸为弱酸,离子方程式中需要保留分子式;
C、铁与稀硝酸反应生成是一氧化氮气体,不会生成氢气;
D、氢氧化钡为易溶物,离子方程式中写成离子形式.
解答:
解:A、氧化铜与稀硫酸反应生成硫酸铜和水,反应的离子方程式为:CuO+2H+=Cu2++H2O,故A正确;
B、醋酸为弱电解质,离子方程式应该保留分子式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,故B错误;
C、稀硝酸为氧化性的酸,铁与稀硝酸反应生成的是一氧化氮气体,如铁过量,反应的离子方程式为:3Fe+2NO3-+8H+=3Fe2+++2NO↑+4H2O,故C错误;
D、氢氧化钡与盐酸发生中和反应,氢氧化钡应该写成离子形式,正确的离子方程式为:OH-+H+=H2O,故D错误;
故选A.
B、醋酸为弱电解质,离子方程式应该保留分子式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,故B错误;
C、稀硝酸为氧化性的酸,铁与稀硝酸反应生成的是一氧化氮气体,如铁过量,反应的离子方程式为:3Fe+2NO3-+8H+=3Fe2+++2NO↑+4H2O,故C错误;
D、氢氧化钡与盐酸发生中和反应,氢氧化钡应该写成离子形式,正确的离子方程式为:OH-+H+=H2O,故D错误;
故选A.
点评:本题考查了离子方程式的正误判断,题目难度中等,该题侧重对学生能力的培养和训练,完成本题需要明确判断离子方程式常用方法(1)检查反应能否发生;(2)检查反应物、生成物是否正确;(3)检查各物质拆分是否正确;(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等);(5)检查是否符合原化学方程式,然后灵活运用即可.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列化学用语正确的是( )
| A、乙烯的结构简式为:CH2CH2 |
| B、苯的分子式为:C6H6 |
| C、羟基的电子式为:-O-H |
D、甲烷分子的比例模型: |
已知:Ni+CuSO4=NiSO4+Cu Cu+2AgNO3=Cu(NO3)2+2Ag 则下列判断正确的是( )
| A、还原性:Ni>Cu>Ag |
| B、氧化性:Ni2+>Cu2+>Ag+ |
| C、还原性:Ni<Cu<Ag |
| D、氧化性:Ni2+<Cu2+<Ag+ |
用NA表示阿佛加德罗常数,下列说法正确的是( )
| A、标准状况下,2.24L水所含的分子数为0.1 NA |
| B、16 g O2含有的氧原子数为NA |
| C、0.3 mol/L的MgCl2溶液中含Mg2+数目为0.3 NA |
| D、22.4L H2中含有的氢分子数为NA |
 Q、R、T、X、Y五种元素的原子序数依次递增,Y的原子序数为29,R、T、X在周期表中的位置如右图所示.R原子基态时2p原子轨道上有3个未成对的电子,Q、X 分别得到一个电子后均形成稀有气体原子的稳定结构.请回答下列问题:
Q、R、T、X、Y五种元素的原子序数依次递增,Y的原子序数为29,R、T、X在周期表中的位置如右图所示.R原子基态时2p原子轨道上有3个未成对的电子,Q、X 分别得到一个电子后均形成稀有气体原子的稳定结构.请回答下列问题:
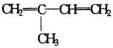 与 CH2=CH2 发生加成反应产物的结构简式(或键线式)
与 CH2=CH2 发生加成反应产物的结构简式(或键线式)