题目内容
17.我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C═K2S+N2↑+3CO2↑.(1)用双桥法标出电子转移的方向及数目:
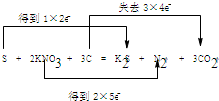
(2)该反应中还原剂是C,氧化剂是S、KNO3.
分析 S+2KNO3+3C═K2S+N2↑+3CO2↑中,S、N元素的化合价降低,C元素的化合价升高,该反应转移12e-,以此来解答.
解答 解:(1)S、N元素的化合价降低,C元素的化合价升高,该反应转移12e-,则用双桥法标出电子转移的方向及数目为 ,
,
故答案为: ;
;
(2)C元素的化合价升高,则还原剂为C,S、N元素的化合价降低,则氧化剂为S、KNO3,故答案为:C;S、KNO3.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念、转移电子及分析与应用能力的考查,题目难度不大.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
8.化学与社会、生产、生活密切相关,下列说法正确的是( )
| A. | 二氧化硫可广泛用于食品的漂白 | |
| B. | 从海水提取物质都必须通过化学反应才能实现 | |
| C. | 葡萄糖可用于补钙药物的合成 | |
| D. | “地沟油”禁止食用,也不能用来制肥皂 |
5.下列说法正确的是( )
| A. | 杂化轨道全部参加形成化学键 | |
| B. | 在晶体中,只要有阴离子一定有阳离子 | |
| C. | 某固态单质能导电,该单质一定属于金属晶体 | |
| D. | SiO2分子中每个Si原子周围有4个O原子,每个O原子周围有2个Si原子 |
12.已知下列几个反应的化学方程式:①2KI+Cl2═2KCl+I2、②2FeCl2+Cl2═2FeCl3、③2FeCl3+2HI═2FeCl2+I2+2HCl,下列有关物质的氧化性的强弱排列顺序中正确的是( )
| A. | Cl2>Fe3+>I2 | B. | Cl2>I2>Fe3+ | C. | Fe3+>Cl2>I2 | D. | Fe3+>I2>Cl2 |
2.下列关于中和热测定实验的叙述正确的是( )
| A. | 为使反应充分进行,应将盐酸分次加入碱液中 | |
| B. | 为使反应刚好完全进行,应使用浓度和体积相同的NaOH和HCl溶液 | |
| C. | 测量初始温度时,测量盐酸后需清洗温度计再测量NaOH溶液温度 | |
| D. | 如无玻璃环形搅拌棒,可利用铁丝或铜丝代替 |
9.取Fe、FeO、Fe2O3的均匀混合物质量为6.4g,向其中加入200mL 1mol•L-1的盐酸,恰好使混合物完全溶解,放出1120mL(标准状况)的气体.所得溶液中,加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,并将产生的CO通入过量澄清石灰水中,生成沉淀的质量为( )
| A. | 2.5g | B. | 5.0g | C. | 7.5g | D. | 10.0g |
6.化学与生产、生活密切相关,下列表述错误的是( )
| A. | 使用新能源,减少化石燃料的燃烧,可防止酸雨的产生 | |
| B. | 明矾在水中能形成胶体,可作为净水剂 | |
| C. | 建设三峡大坝使用了大量水泥,水泥是硅酸盐材料 | |
| D. | 给汽车安装尾气转化装置,易产生光化学烟雾 |
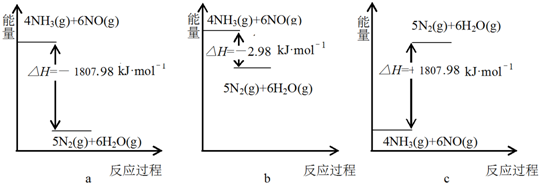
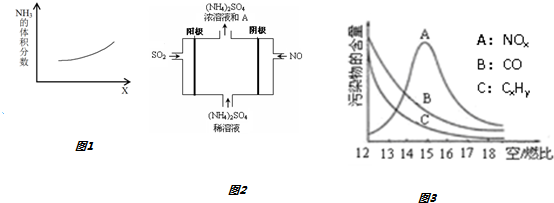
 .
.