题目内容
下列方程式书写正确的是
A.HCO3-在水溶液中的电离方程式:HCO3- +H2O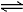 H3O++CO32-
H3O++CO32-
B.H2SO3的电离方程式H2SO3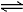 2H++SO32-
2H++SO32-
C.CO32-的水解方程式:CO32- +2H2O H2CO3+2OH-
H2CO3+2OH-
D.CuSO4的水解方程式: Cu2++2H2O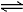 Cu(OH)2+2H+
Cu(OH)2+2H+
AD
【解析】
试题分析:A.HCO3-是弱酸的酸式酸根离子,所以在水溶液中的存在电离平衡,电离方程式:HCO3- +H2O H3O++CO32-,错误;B.H2SO3是二元弱酸,在溶液中分步电离,电离方程式H2SO3
H3O++CO32-,错误;B.H2SO3是二元弱酸,在溶液中分步电离,电离方程式H2SO3 H++HSO3-,错误;C.碳酸是二元弱酸,在溶液中CO32-的水解是分步水解的,水解的离子方程式:CO32- +H2O
H++HSO3-,错误;C.碳酸是二元弱酸,在溶液中CO32-的水解是分步水解的,水解的离子方程式:CO32- +H2O HCO3-+OH-;错误;D.CuSO4是可溶性强电解质,在溶液中Cu2+的水解方程式: Cu2++2H2O
HCO3-+OH-;错误;D.CuSO4是可溶性强电解质,在溶液中Cu2+的水解方程式: Cu2++2H2O Cu(OH)2+2H+,正确。
Cu(OH)2+2H+,正确。
考点:考查盐的水解和若电解质的电离方程式的书写正误的判断的知识。

练习册系列答案
相关题目






 2CrO42- +2H+的影响,往5mL 0.1mol/L K2CrO4溶液加入5mL 0.1mol/L的稀硫酸
2CrO42- +2H+的影响,往5mL 0.1mol/L K2CrO4溶液加入5mL 0.1mol/L的稀硫酸