题目内容
(4分)(1)12.4gNa2X中含0.4mol Na+,则Na2X的摩尔质量是 。
(2)将密度为1.84g/cm3、质量分数为98%的浓硫酸稀释成1000ml、物质的量浓度为2mol/L、密度为1.20g/cm3的稀硫酸。所需浓硫酸的体积为 。
(4分) (1)62g/mol (2)108.7mL (每空2分)
【解析】
试题分析:(1)盐电离方程式是Na2X=2Na++X2-,可见1mol的盐电离会产生2mol的Na+。现在Na+的物质的量是0.4mol,则盐的物质的量是0.2mol.n=m/M,所以M=m/n=12.4g÷0.2mol=62g/mol;(2)溶液在稀释前后溶质的物质的量不变。在稀释前溶质的物质的量浓度是C=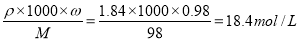 ,由于C1? V1=c2?V2;所以V1= c2?V2/ C1=(1000ml× 2mol/L) ÷18.4mol/L=108.7mL.
,由于C1? V1=c2?V2;所以V1= c2?V2/ C1=(1000ml× 2mol/L) ÷18.4mol/L=108.7mL.
考点:考查物质的量的有关计算的知识。

练习册系列答案
相关题目
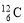 、
、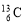 、
、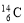 的说法正确的是
的说法正确的是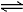 H3O++CO32-
H3O++CO32- H2CO3+2OH-
H2CO3+2OH-