题目内容
已知甲、乙两种有机物的结构简式为:
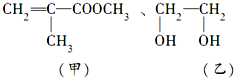
(1)甲中不含氧原子的官能团是 ,乙中含有的官能团是 .
(2)写出下列反应的化学方程式:①甲与溴水的反应: .
②1mol乙与2mol醋酸发生酯化反应 .
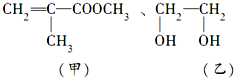
(1)甲中不含氧原子的官能团是
(2)写出下列反应的化学方程式:①甲与溴水的反应:
②1mol乙与2mol醋酸发生酯化反应
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:(1)甲中不含氧原子的官能团为碳碳双键,含氧官能团为酯基;乙中含有的官能团为-OH;
(2)①甲中含C=C,与溴水发生加成反应;
②1mol乙中含2mol-OH,与2mol醋酸发生酯化反应生成酯和2molH2O.
(2)①甲中含C=C,与溴水发生加成反应;
②1mol乙中含2mol-OH,与2mol醋酸发生酯化反应生成酯和2molH2O.
解答:
解:(1)(1)甲中不含氧原子的官能团为碳碳双键,含氧官能团为酯基;乙中含有的官能团为-OH,名称为羟基,
故答案为:碳碳双键;羟基(或-OH);
(2)①甲中含C=C,与溴水发生加成反应,该反应为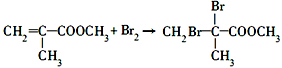 ,
,
故答案为: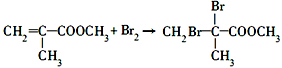 ;
;
②1mol乙中含2mol-OH,与2mol醋酸发生酯化反应生成酯和2molH2O,该反应为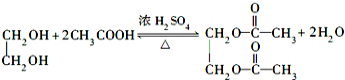 ,
,
故答案为: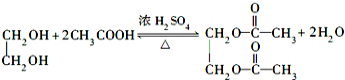 .
.
故答案为:碳碳双键;羟基(或-OH);
(2)①甲中含C=C,与溴水发生加成反应,该反应为
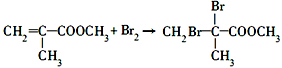 ,
,故答案为:
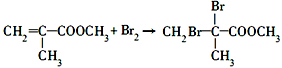 ;
;②1mol乙中含2mol-OH,与2mol醋酸发生酯化反应生成酯和2molH2O,该反应为
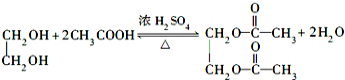 ,
,故答案为:
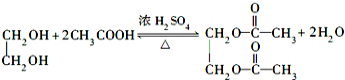 .
.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、羧酸、醇性质的考查,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
将11.2gFe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到40g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在密闭容器中高温加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为( )
| A、2240mL |
| B、4480mL |
| C、3360mL |
| D、1120mL |
已知短周期元素的离子aW3+、bX+、cY2-、dZ-具有相同的电子层结构,下列关系正确的是( )
| A、质子数c>b |
| B、原子半径X<W |
| C、氢化物的稳定性H2Y>HZ |
| D、离子的还原性Y2->Z- |
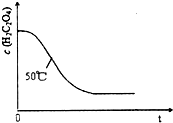
下列反应前后物质的总能量变化可用如图表示的是( )
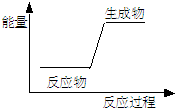

| A、生石灰加水生成熟石灰 |
| B、C+H2O═CO+H2 |
| C、金属钠与水反应 |
| D、HNO3+NaOH═NaNO3+H2O |
可以用分液漏斗分离的一组混合物是( )
| A、酒精和碘 | B、溴和四氯化碳 |
| C、乙酸和水 | D、苯和水 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、17g羟基(-OH)所含有的电子数是10NA个 |
| B、1mol苯乙烯中含有的碳、碳双键数为4NA个 |
| C、常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
| D、4.2g C3H6中含有的碳碳双键数一定为0.1NA |