题目内容
12.下列物质的水溶液能在蒸发皿中蒸干灼烧得到原物质的是( )①FeCl3②绿矾③碳酸氢钠 ④Na2SO3 ⑤KNO3 ⑥CaCl2 ⑦HCl.
| A. | ⑤⑥ | B. | ②③④⑤ | C. | ③⑤ | D. | ①③⑤ |
分析 从盐类水解的角度和物质的稳定性的角度分析,注意当水解生成挥发性酸时,加热蒸干并灼烧最终得到的是金属氧化物,另外,加热易分解、易氧化的物质不能得到原物质,以此解答该题.
解答 解:①FeCl3溶液加入水解生成氢氧化铁和盐酸,盐酸挥发,灼烧生成氧化铁,故错误;
②绿矾主要成分为硫酸亚铁,加热过程中被氧化为硫酸铁,故错误;
③碳酸氢钠不稳定,加热易分解,蒸干得到分解产物碳酸钠,故错误;
④Na2SO3具有还原性,加热过程中被氧化为硫酸钠,故错误;
⑤硝酸钾不会发生水解,蒸干得到原物质,故正确;
⑥CaCl2不水解,较稳定,蒸干得到原物质,故正确;
⑦HCl易挥发,蒸干得不到任何物质,故错误;
则能得到原物质的是⑤⑥.
故选A.
点评 本题考查盐类水解的应用,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意盐类水解的原理,特别是能把握相关物质的性质.

练习册系列答案
相关题目
20.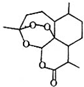 屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
 屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | B. | 青蒿素是芳香族化合物 | ||
| C. | 青蒿素可以发生水解反应 | D. | 青蒿素不能使酸性KMnO4溶液褪色 |
4.工业焊接钢管常用55137Cs进行“无损探伤”.下列有关说法正确的是( )
| A. | 137表示质量数 | B. | 137表示质子数 | ||
| C. | 该原子质子数大于中子数 | D. | 55表示中子数 |
2.某学生在做元素性质与原子结构关系的实验时,设计了一套实验方案,并记录了有关的实验现象.请帮助该学生整理并完成实验报告.
(1)实验目的:探究同一主族元素性质的递变规律.
(2)实验用品:仪器:试管、胶头滴管.
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳.
(3)实验内容(在下表横线中填写相关内容).
(4)实验结论:同主族元素从上到下元素原子的得电子能力逐渐减弱.
(5)问题和讨论.
①上述两个实验中发生反应的离子方程式分别为Cl2+2Br-=Br2+2Cl-、2I-+Br2=2Br-+I2.
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱.试列举两项事实说明氟的非金属性比氯的强:HF的稳定性比HCl强、F2能置换出水中的氧,而Cl2不能置换出水中的氧.
(1)实验目的:探究同一主族元素性质的递变规律.
(2)实验用品:仪器:试管、胶头滴管.
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳.
(3)实验内容(在下表横线中填写相关内容).
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层 呈橙红色 |
| ② | 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层 呈紫红色 |
(5)问题和讨论.
①上述两个实验中发生反应的离子方程式分别为Cl2+2Br-=Br2+2Cl-、2I-+Br2=2Br-+I2.
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱.试列举两项事实说明氟的非金属性比氯的强:HF的稳定性比HCl强、F2能置换出水中的氧,而Cl2不能置换出水中的氧.
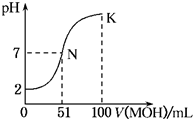 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: