��Ŀ����
��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ���������ԭ�Ӽ��γ�1mol��ѧ��ʱ�ͷŵ�������Ͽ�1mol��ѧ��ʱ�����յ����������ṩ���»�ѧ���ļ��ܣ�kJ/mol��P�DP��198 P�DO��360 O=O��498 P=O��585
�Ը�����Щ���ݣ��������·�Ӧ��Q
P4�����ף�(g) + 5O2(g) = P4O10(g)�� ��H=�DQ kJ/mol
����ʾ�����������������͵ķ��ӣ��������γ�P4O10ʱ��ÿ������ԭ��֮�����һ����ԭ�ӣ�����ÿ����ԭ������˫�����һ����ԭ�ӣ�
-Q = 198��6+498��5-12��360-4��585, ��Q=2982

��ϰ��ϵ�д�
 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д� Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�����Ŀ
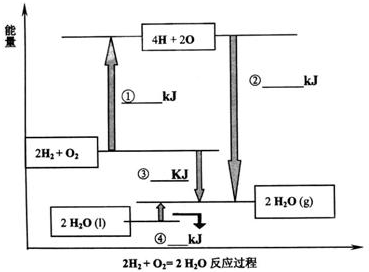
 ��1����25�桢101kPa״���£�4g����������������Ӧ����1molˮ��������241.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��
��1����25�桢101kPa״���£�4g����������������Ӧ����1molˮ��������241.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��2011?����ģ�⣩��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪���ף�P4����P4O6�ķ��ӽṹ��ͼ��ʾ��
��2011?����ģ�⣩��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪���ף�P4����P4O6�ķ��ӽṹ��ͼ��ʾ�� ��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���֪�Ͽ�1mol���л�ѧ��ʱ��Ҫ���յ������ֱ�Ϊ��P-P 198kJ��P-O 360kJ��O=O 498kJ
��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���֪�Ͽ�1mol���л�ѧ��ʱ��Ҫ���յ������ֱ�Ϊ��P-P 198kJ��P-O 360kJ��O=O 498kJ